题目内容
【题目】甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如下所示:
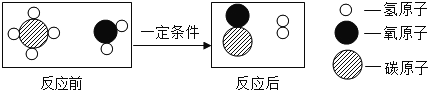
根据以上微观示意图得出的结论中,正确的是
A.反应前后各元素的化合价均不变
B.水煤气的成分是一氧化碳和氧气
C.该反应中含氢元素的化合物有3种
D.该反应的化学方程式中甲烷和水的计量数之比为1:1
【答案】D
【解析】
试题分析:A.反应前后各元素的化合价均不变是错误的叙述,因为反应后由单质氢气生成;B选项水煤气的成分是一氧化碳和氧气,根据题中图标可知是错误的叙述,水煤气的成分是一氧化碳和氢气;C选项该反应中含氢元素的化合物有3种是错误的叙述,该反应中含氢元素的化合物有2种,一种是单质;D选项该反应的化学方程式中甲烷和水的计量数之比为1:1,根据质量守恒定律可知是正确的叙述,故答案选择D

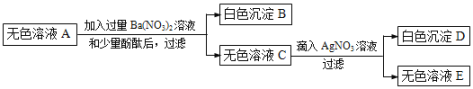
【题目】根据下图回答问题。
请从A或B两题中任选1个作答,若两题均作答,按A计分。
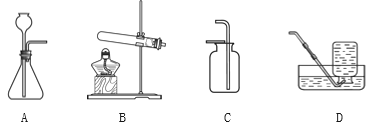
A | B |
(1)实验室制取CO2化学方程式 为______。 (2)CO2可以用______(填序号) 装置收集。 | (1)实验室用高锰酸钾制取 O 2 选 取的发生装置是_______。 (2)化学方程式为______。 |
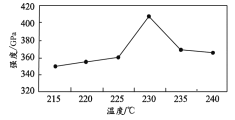
【题目】某实验小组用石墨做电极进行电解水实验,为增加导电性,改用Ca(OH)2饱和溶液进行电解,实验时除两个电极均有气泡冒出外,溶液中还出现了白色浑浊,该小组对白色浑浊出现的原因进行了如下探究。
(猜想与假设)
① 溶液温度升高导致Ca(OH)2析出而出现白色浑浊。
② 水减少导致Ca(OH)2析出而出现白色浑浊。
③ 与石墨电极有关。
(查阅资料)
① Ca(OH)2的溶解度:20℃时为0.16 g,100℃时为0.07 g。
② 在加热条件下铜能与氧气反应生成黑色的氧化铜。铜与稀硫酸不反应;氧化铜能与稀硫酸反应。
(进行实验)
实验 | 实验装置 | 主要实验操作 | 实验现象 |
1 | 取20mLCa(OH)2 饱和溶液加热至沸腾 | 溶液中未出现白色浑浊 | |
2 |
| 取Ca(OH)2饱和溶液于烧杯中,加5 ml水,通电3 min | 烧杯中溶液体积几乎无明显变化,溶液中明显出现白色浑浊 |
3 | 更换石墨电极为铜电极,取Ca(OH)2 饱和溶液于烧杯中,通电3 min | 与电源正极相连的铜电极变黑,溶液中未出现白色浑浊 |
(解释与结论)
(1)实验1得出的结论是_______。
(2)实验2通电3 min后得到的溶液为_______(填“饱和”或“不饱和”)溶液。
(3)猜想与假设②不成立,依据的现象是_______。
(4)实验3中更换石墨电极为铜电极的目的是_______。
(反思与评价)
(5)为除去实验3中铜电极上的黑色物质,需要的试剂是______。
(6)通过探究过程,用石墨做电极进行实验时,Ca(OH)2溶液中出现白色浑浊的原因是_______。