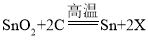题目内容
【题目】一定质量的氯化钡溶液和100g溶质质量分数为9.8%的稀硫酸恰好完全反应,过滤得到284.7g溶液。计算:
(1)生成硫酸钡沉淀的质量为多少?
(2)氯化钡溶液中的溶质质量分数为多少?(精确到0.1%)
【答案】(1)23.3g(2)![]()
【解析】
已知参加反应的硫酸质量,根据化学方程式进行计算求出生成物硫酸钡的质量,
解:(1)由题意可知参加反应的硫酸质量=100g×9.8%=9.8g,
设生成硫酸钡沉淀的质量为x,参加反应的氯化钡质量为y,
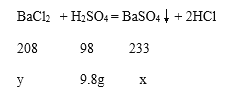
![]() =
=![]() 解得x=23.3g
解得x=23.3g
![]() =
=![]() 解得y=20.8g
解得y=20.8g
(2)根据质量守恒定律可知,反应前氯化钡溶液的质量=23.3g+284.7g-100g=208g,则氯化钡溶液的溶质质量分数=![]() ×100%=10.0%,
×100%=10.0%,
答:(1)生成硫酸钡沉淀的质量为23.3g;(2)氯化钡溶液中的溶质质量分数为10.0%。

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
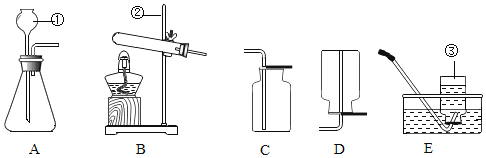
【题目】下图为实验室制氧气的装置图。请从A或B两题中任选一个作答,若两题均作答,按A计分。
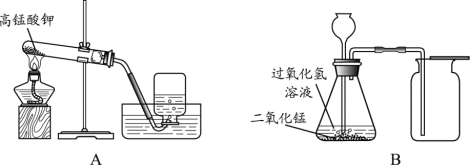
A | B |
(1)A图中反应的化学方程式为________。 (2)O2可用排水法收集,其原因是________。 | (1)B图中反应的化学方程式为________。 (2)B中长颈漏斗底端伸入液体内的原因是________。 |
【题目】某同学为探究铁合金中铁的质量分数,先后进行了三次实验,实验数据如下表:
实验次数 项目 | 第一次 | 第二次 | 第三次 |
所取合金的质量/g | 20 | 20 | 40 |
所加稀硫酸的质量/g | 100 | 120 | 80 |
生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的铁恰好完全反应时,消耗稀硫酸溶液的质量是_____g.
(2)该铜铁合金中铁的质量分数是多少?_____。