题目内容
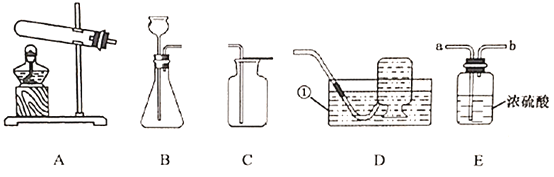
【题目】如图中A是氟元素在元素周期表中的相关信息,BF是某些粒子的结构示意图。请回答:
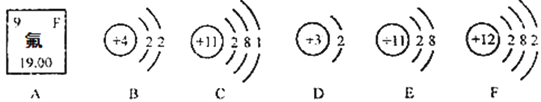
(1)氟的相对原子质量是_____。
(2)B﹣F中属于同种元素的是_____(填字母,下同)。
(3)与B化学性质相似的是_____。
(4)F在化学反应中易_____(选填“得到”或“失去”)电子。
【答案】 19.00 CE F 失去
【解析】
本题考查了微粒结构示意图,元素周期表的特点及其应用。可根据元素周期表中汉字下面的数字表示相对原子质量,质子数相同的原子属于同一种元素,元素的化学性质跟它的原子的最外层电子数目有关,决定元素的化学性质的是原子的最外层电子数进行分析解答。
(1)根据氟元素周期表中的一格中获取的信息,元素周期表中汉字下面的数字表示相对原子质量,氟的相对原子质量是19.00;
(2)质子数相同的原子属于同一种元素,由图可知B﹣F中属于同种元素的是C、E;
(3)决定元素的化学性质的是原子的最外层电子数,F粒子、B粒子的最外层电子数相同,F粒子化学性质与B粒子化学性质相似;
(4)F的最外层电子数为2,小于4个,在化学反应中易失去电子。

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
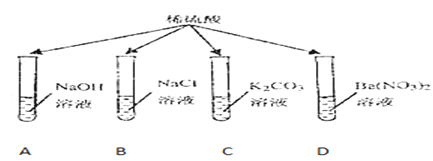
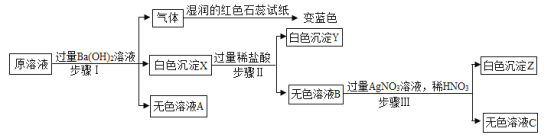
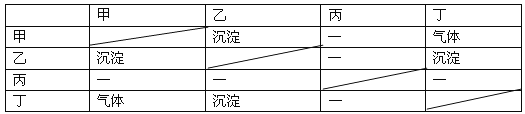
鸿图图书寒假作业假期作业吉林大学出版社系列答案【题目】兴趣小组为探究某些酸碱盐之间能否发生反应,进行了如图所示的实验:把稀硫酸分别加入到盛有不同药品的A、B、C、D四只试管中。请回答:
(1)甲同学观察到A、B试管中均无明显现象,于是得出结论:硫酸与氢氧化钠及氯化钠都不能发生反应。乙同学认为A试管中发生了反应,理由是_____。(用化学方程式表示)。B试管中不能发生复分解反应,理由:_____。
(2)丙同学观察到C试管中有_____生成,于是得出结论:硫酸与碳酸钾能发生反应。
(3)丙同学对反应后C试管中溶液的溶质成分进行分析得出如下结论:
结论一:K2SO4 结论二:K2SO4、H2SO4 结论三:_____
丙同学设计实验,用两种方法验证结论三正确:
实验操作 | 实验现象 | 实验结论 |
方法一:取C中溶液少许,加入足量的BaCl2溶液 | 产生白色沉淀 | 结论三正确 |
方法二:取C中溶液少许,加入适量的_____ | 产生气泡 |
乙同学对方法一提出质疑,认为方法一不正确,理由是_____。
(4)丁同学观察到D试管中有白色沉淀生成,于是得出结论:硫酸与硝酸钡能发生反应。写出该反应的化学方程式_____。