题目内容
【题目】化学课上,同学们做了人体呼出的气体使澄清石灰水变浑浊的实验后,对呼出的气体中主要成分及含量非常好奇,设计实验进行探究。
(提出问题)呼出的气体中有哪些主要成分,它们的含量是多少?
(查阅资料)①呼出的气体中仍含有O2。
②CO2在饱和NaHCO3溶液中的溶解度非常小。
(猜想与实验)
猜想:呼出的气体中主要成分是N2、O2、CO2、水蒸气等。
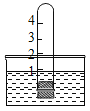
实验I:验证呼出的气体中含有水蒸气。
(1)实验操作如图所示。
(2)观察到的现象为________,根据该现象可以判断呼出的气体中含有水蒸气。
实验II:验证呼出的气体中含有N2、O2、CO2,并测定其含量。
同学们在老师的指导下设计了如下图所示装置(B是带刻度的量气装置)。
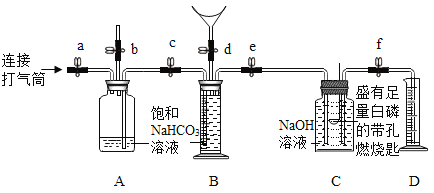
(1)实验记录
实验操作 | 主要实验现象 | 实验结论及解释 | |
① | 检查装置的气密性。 向装置中加入药品。 关闭止水夹a~f。 | 装置的气密性良好。 | |
② | 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温。 | B中液体进入到A中,B中液体减少500 mL。 | 收集500 mL气体。 |
③ | 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出。 | ________,D中液体为475 mL。 | 反应的化学方程式为________。 |
④ | 关闭e、f,用凸透镜聚光引燃白磷。 | 白磷燃烧,产生大量白烟,放出大量热。 | 呼出的气体中含有O2。 |
⑤ | 待白磷熄灭并冷却到室温,打开f。 | ________,D中剩余液体为400 mL。 | 呼出的气体中含有N2。 |
(2)数据处理
呼出的气体中主要成分的含量
N2 | O2 | CO2 | |
体积/mL | |||
体积分数/% |
同学们经过3次重复实验,确认了呼出气体中的主要成分及其含量。
(实验反思)
(1)该实验设计依据的N2性质有 (填字母序号)。
A.难溶于水 B.不能和NaOH溶液反应
C.无色无味的气体 D.不能燃烧,也不支持燃烧
(2)实验II操作⑤中,若C中气体未完全冷却就打开f并读数,则所测O2的体积分数(填“偏小”、“不变”或“偏大”)。
【答案】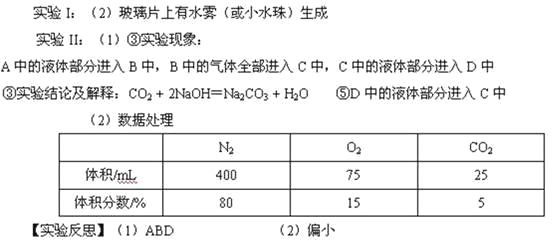
【解析】
【猜想与实践】(2)根据所做的实验来判断实验现象;
实验记录:③向A中充气会使液体被重新压回B中,从而将气体排放到C中,而其中二氧化碳可以和氢氧化钠发生反应,可以据此解答该题;
⑤白磷燃烧要消耗氧气,从而会使C装置中的压强变小,而使D中的液体倒吸入C装置中,可以据此填空;
数据处理:根据各步骤所消耗的气体来计算,并完成解答;
【实验反思】(1)根据实验过程所设计的物质及反应条件来判断氮气的性质;
(2)根据气体受热膨胀的知识点来解答该题.
解答:解:【猜想与实践】(2)对着玻璃呼气会使呼出气体中的水蒸气遇冷而凝结成水,所以会在玻璃的表面产生一层水雾.
实验记录:③关闭b向A装置中通入气体,则会使A中的液体被压入B装置中,从而使B中的液面上升,而使B中的气体被压入C中,所以在C导管口会发现有气泡冒出,由于气体中含有二氧化碳,所以由于二氧化碳要和氢氧化钠,但是大部分气体不会发生反应而滞留在C装置中,将C装置中的液体压入D中;
⑤白磷燃烧要消耗氧气,从而会使C装置中的压强变小,而使D中的液体倒吸入C装置中,是C装置中的液面上升;
数据处理:根据将气体鼓入C装置后气体体积减少了25mL可以知道该气体为二氧化碳,而白磷燃烧后气体体积剩余了400mL,结合气体的性质可以判断出这400mL气体为氮气,被消耗的体积为75mL,即氧气的体积为75mL,进而可以求出氮气的体积分数为:
![]() ×100%=80%,氧气的体积分数为:
×100%=80%,氧气的体积分数为:
![]() ×100%=15%,二氧化碳的体积分数为:
×100%=15%,二氧化碳的体积分数为:
![]() ×100%=5%;
×100%=5%;
【实验反思】(1)根据实验过程中所接触的物质及反应条件可以知道,氮气不能燃烧也不支持燃烧,难溶于水,并且不能和氢氧化钠溶液反应,虽然能够观察出氮气是无色气体,但是闻不到氮气的气味,所以题中所给的ABD选项是正确的,故选ABD;
(2)如果C装置没有完全冷却即打开止水夹f,则会由于C中温度较高气体受热膨胀,而使D中液体进入到C中减少,D中剩余液体大于400mL,即氧气会小于100mL.则所测O2的体积分数会偏小.
故答案为【猜想与实践】(2)玻璃片表面有一层水雾
实验记录:故答案为【猜想与实践】(2)玻璃片表面有一层水雾
实验记录:
实验操作 | 主要实验现象 | 实验结论及解释 | |
① | 检查装置的气密性.向装置中加入药品.关闭止水夹a~f. | \ | 装置的气密性良好. |
② | 打开b、c、d,向B中吹入一定量气体后关闭d,并冷却到室温. | B中液体进入到A中,B中液体减少500mL. | 收集500mL气体. |
③ | 关闭b,打开a、e、f,用打气筒向A中缓缓充气,直到B中气体刚好全部排出. | A中液面下降,B中液面上升至最高,C中左侧导管口有气泡产生,且C中液面下降,液体沿导管流入D中,D中液体为475mL. | 反应的化学方程式为 CO2+2NaOH═Na2CO3+H |
④ | 关闭e、f,用凸透镜聚光引燃白磷. | 白磷燃烧,产生大量白烟,放出大量热. | 呼出的气体中含有O2. |
⑤ | 待白磷熄灭并冷却到室温,打开f. | D中液体倒吸入C瓶中,C瓶中液面上升,D中剩余液体为400mL. | 呼出的气体中含有N2. |
数据处理(2)
N2 | O2 | CO2 | |
体积/mL | 400 | 75 | 25 |
体积分数/% | 80 | 15 | 5 |
实验反思(1)ABD;
(2)偏小.

【题目】化学兴趣小组为验证质量守恒定律,按照如图装置进行实验,称取24g镁粉在空气中燃烧,发现产物中有少量黄色固体。
[提出问题]黄色固体是什么呢?
[查阅资料]①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
[做出猜想]黄色固体是Mg3N2。
[实验探究]请设计实验,验证猜想。
实验操作 | 实验现象及结论 |
取燃烧后的产物于试管中,加少量_________,再将______放在试管口,观察现象 | 观察到________,说明燃烧产物中含有Mg3N2 |
[反思与交流](1)Mg3N2中氮元素的化合价为________。
(2)空气中N2的含量远大于O2的含量,而镁粉在空气中燃烧生成的MgO却远多于Mg3N2,其原因是_______。
(3)写出镁粉在氮气中燃烧的化学方程式_______。
(4)镁粉还可以在CO2中燃烧,反应生成一种白色氧化物和一.种黑色固体,写出该反应的化学方程式:________。
【题目】密闭容器中,下列各组物质在一定条件下充分反应后,冷却至室温,密闭容器中的气态物质为纯净物的是( )
A.分子数比为1:1的![]() 和
和![]() B.物质的量比为4:3的
B.物质的量比为4:3的![]() 和
和![]()
C.质量比为1:5的![]() 和
和![]() D.质量比为3:8的
D.质量比为3:8的![]() 和
和![]()
【题目】探究石灰石煅烧实验。
(1)煅烧石灰石发生反应的化学方程式是_____。
(2)欲证明石灰石煅烧生成二氧化碳,下列实验中可行的是_____(填编号)。
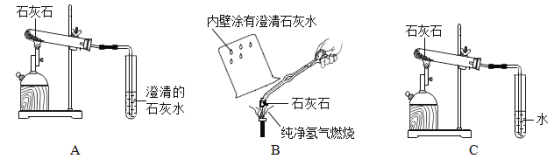
(3)为探究石灰石煅烧后的分解情况,去煅烧后的固体分别做了四个实验:
实验编号 | 实验操作 | 现象 |
甲 | 取样于试管中,加水 | 白色不溶物 |
乙 | 取样于试管中,先加水,再滴加酚酞 | 白色不溶物,红色溶液 |
丙 | 取样于试管中,先加水,再通入少量二氧化碳 | _____ |
丁 | 取样于试管中,加足量稀盐酸 | 有气泡 |
I、能证明石灰石部分分解的实验是_____(填实验编号)。
II、乙实验中白色不溶物中所含的钙元素质量_____(选填“大于”“等于”“小于”)煅烧前石灰石中 钙元素质量。