题目内容
【题目】2017年11月发布的全球超级计算500强,我国“神威太湖之光”第四次夺冠,其电脑芯片的主要原料是沙子,这些沙子经过数千摄氏度的高温和化学药品的净化转变成完全纯净的硅柱,而美国加利福尼亚的“硅谷”名称就由此得来。工业上生产硅的过程如图:
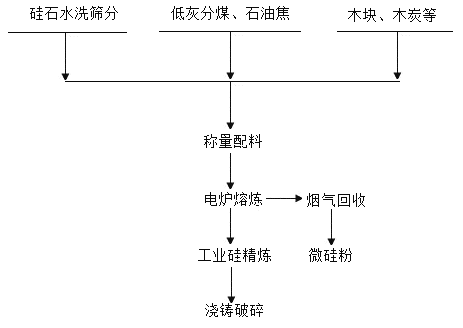
(1)硅石主要成分为SiO2,SiO2与木炭在高温条件下反应生成硅和CO,请写出化学方程式:_____;
(2)反应中产生的气体主要成分为CO、CO2、CH4、H2、O2,请写出其中一种气体处理或转化的方法_____;
(3)在硅的精炼过程中要除去的杂质包括:Al、CaO和Al2O3,利用所学化学知识可知,加入足量_____类(填“酸”、“碱”或“盐”)物质可将其除去。
(4)在2020年前,也许就不用硅制造CPU了,因为晶体管的大小快达到硅的物理极限了,硅也将被新材料替代。而考虑到金属矿物有限,且不能再生,目前已广泛使用_____来替代金属材料了。
【答案】
 (合理均可) 酸类 塑料
(合理均可) 酸类 塑料
【解析】
(1)二氧化硅和木炭在高温的条件下生成硅和一氧化碳,化学方程式为 ;
;
(2)一氧化碳和氧气在点燃的条件下生成二氧化碳,化学方程式为 ;
;
(3)金属、金属氧化物会与酸反应,所以加入足量酸类物质可将其除去;
(4)塑料属于可再生资源,所以考虑到金属矿物有限,且不能再生,目前已广泛使用塑料来替代金属材料了。

【题目】胃舒平(含Al(OH)3)、小苏打片(含NaHCO3)、胃酸抑制剂(主要含CaCO3、Mg(OH)2)都是常用的中和胃酸的药物。
(1)胃舒平与胃酸发生反应的化学方程式为:_____。
(2)为了探究工业小苏打中是否含少量的NaCl,设计如下实验:(假设小苏打片中其他物质均不含Cl-)
实验步骤 | 实验现象 | 实验结论 |
第一步:取1片小苏打于试管中,加入适量水充分溶解,再滴加足量的稀HNO3。 | 有_____产生 | 说明小苏打片中含有NaHCO3。 |
第二步:再往上述溶液中滴加少量_____溶液。(写化学式) | 有_____产生 | 说明小苏打片中含有NaCl。 |
(3)胃酸抑制剂每片lg,取10片于烧杯中,再加入50g稀HCl,烧杯中剩余物的质量与时间的关系如下表:(已知其他物质不与稀盐酸反应)
时间/s | 0 | 10 | 20 | 30 | 40 | 50 |
剩余物的质量/g | 60 | 59.12 | 58.24 | 57.36 | 56.48 | 56.48 |
求每片胃酸抑制剂中CaCO3的质量分数_____(写出计算过程)。
【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
组合序号 | ① | ② | ③ |
组合的溶液 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 |
实验二


实验二
[实验一]:把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液
(1)写出混合后得到蓝色沉淀一定发生反应的化学方程式_____。
(2)混合后所得无色溶液中一定含有的溶质是_____(填化学式,下同)可能含有的溶质是_____。
[实验二]:
(3)在组合①、②、③中,组合_____无明显现象,但它们的实质不同,为了证明实质不同。小夕在实验过程中使用了酚酞试液
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中除酚酞外溶质的组成可能是_____(填化学式)
[结论]:
(5)复分解反应发生的条件是:生成物中有_____。
【题目】某校实验室有一瓶久置的铁粉,已部分锈蚀,某兴趣小组对其组成进行如下探究:
(1)定性探究:
取样品平铺于白纸上,用磁铁置于样品上方,黑色固体全部被吸起,白纸上留下______色固体;将被磁铁吸起的黑色固体全部投入硫酸铜溶液中,充分反应后,过滤,所得固体全部为红色。样品中含有铁和氧化铁。
(2)定量探究:
按下图所示装置进行实验(装置气密性良好,固定装置已略去;氮气不与铁屑中的成分反应;碱石灰是氧化钙和氢氧化钠的混合物)。
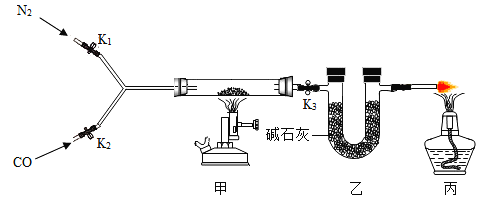
Ⅰ称量硬质玻璃管的质量。将样品放入硬质玻璃管中,称量硬质玻璃管和样品的质量。
Ⅱ连接好装置。缓缓通入N2,燃甲处的酒精喷灯,待硬质玻璃管中固体恒重,记录硬质玻璃管和剩余固体的质量。
Ⅲ再次连接好装置,继续实验。通入CO,点燃丙处的酒精灯和甲处的酒精喷灯。待硬质玻璃管中固体恒重,熄灭酒精喷灯,继续通入CO直至硬质玻璃管冷却。再次记录硬质玻璃管和剩余固体的质量。
数据如下表:
硬质玻璃管 | 硬质玻璃管和样品 | 步骤Ⅱ硬 质玻璃管和剩余固体 | 步骤Ⅲ硬质玻璃管和剩余固体 | |
质量 | m1 | m2 | m3 | m4 |
①步骤Ⅲ丙处酒精灯的作用是_______。
②步骤Ⅲ玻璃管中反应的化学方程式为______。
③样品中氧化铁的质量分数为_______(用m1、m2、m3、m4的代数式表示)。
④若步骤Ⅲ中氧化铁没有完全反应,样品中水的质量分数测量结果将_____(填“偏大”“偏小”或“不变”)。
⑤有关样品,下列说法正确的是_____(填序号,多选)。
A样品中氢元素的质量为![]()
B样品中铁单质和氧化铁的质量总和为m3-m1
C样品中铁单质的质量为m4-m1
D样品中氧元素的质量为m3-m4