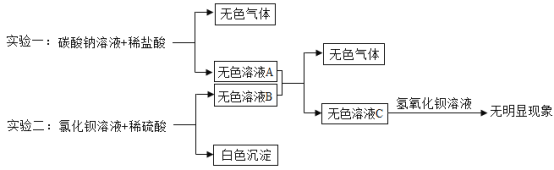
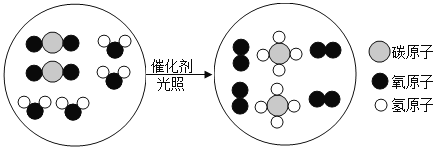
题目内容
【题目】学习化学离不开实验
[实验I ]下图是实验室常用的实验仪器与装置:
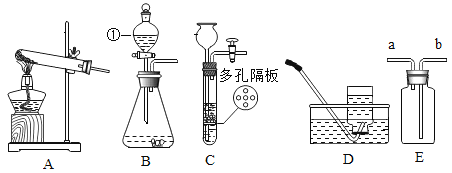
(1)仪器①的名称为___________。
(2)用氯酸钾与二氧化锰制备氧气的发生装置是_____(填序号), 其化学反应方程式为____。
(3)实验室用装置B或C制备CO2,装置C相对于B的优点是________。用装置E收集CO2,气体从b端通入的原因是_________。
(4)某大理石中含有少量硫化物,用该大理石和稀盐酸制得的CO2中混有少量H2S等气体。欲获取纯净干燥的CO2,设计如图所示实验:查阅资料: H2S能与NaOH、CuSO4溶液反应
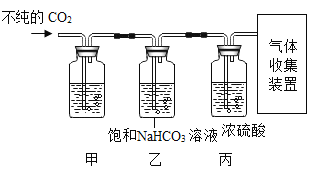
①装置甲中所盛试剂应选用_________( 填字母)。
a NaOH溶液
b 澄清石灰水
c CuSO4溶液
②装置乙的作用是_________。
[实验II ]实验室的pH仪器的电极不用时,常浸泡在饱和KCl溶液里。某同学利用实验室氯酸钾制备氧气后的混合物获得配制上述饱和溶液的KCl晶体。
(5)由混合物获得KCl晶体的主要实验操作步骤为溶解、过滤、_____________。
(6)在上述“过滤”操作中使用玻璃棒的作用是______________。
【答案】分液漏斗 A 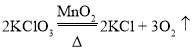 易于控制反应的发生和停止 CO2的密度比空气大 c 除去HCl 蒸发结晶 引流
易于控制反应的发生和停止 CO2的密度比空气大 c 除去HCl 蒸发结晶 引流
【解析】
氯酸钾和二氧化锰加热生成氯化钾和氧气,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳。
(1)仪器①的名称为分液漏斗。
(2)氯酸钾和二氧化锰加热生成氯化钾和氧气,用氯酸钾与二氧化锰制备氧气,需要加热,故发生装置是A,反应的化学反应方程式为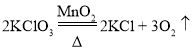 。
。
(3)实验室用装置B或C制备CO2,装置C含有多孔隔板,使固体物质在隔板上,当反应进行时隔板上的固体与液体接触,反应进行;当把止水夹关闭时,产生的气体是压强增大,把液体压入长颈漏斗,隔板上的固体与液体分离,反应停止,故装置C相对于B的优点是易于控制反应的发生和停止。二氧化碳的密度比空气大,二氧化碳从长管通入,空气从短管排出,故用装置E收集CO2,气体从b端通入的原因是CO2的密度比空气大。
(4)①用该大理石和稀盐酸制得的CO2中混有少量H2S等气体,H2S能与CuSO4溶液反应,先要除去硫化氢气体,则装置甲中所盛试剂应选用CuSO4溶液,氢氧化钠和氢氧化钙溶液都会和二氧化碳反应,故选c。
②碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,故装置乙的作用是除去HCl。
(5)由混合物获得KCl晶体的主要实验操作步骤为溶解、过滤、蒸发结晶。
(6)过滤操作中使用玻璃棒的作用是引流。