题目内容
【题目】某兴趣小组做了如下实验.
(实验一)提纯 NaCl
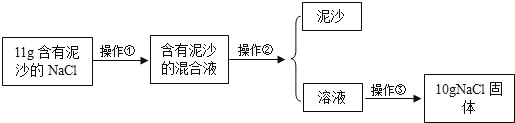
请根据实验回答下列问题:
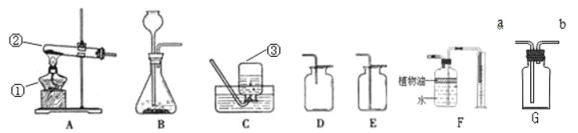
(1)操作①、②、③依次为图中的(填序号)______.
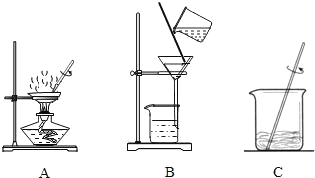
(2)若得到 NaCl 的产率比实际值偏低,则可能的原因是(填序号)_______.
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上
D.溶解 11g 含有泥沙的 NaCl 时,加入的水量不足
(3)用上述实验所得的氯化钠配制溶质质量分数为 5%的氯化钠溶液 50g,不需 要的仪器为(填序号)_____.
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒 精灯
(实验二)溶解和结晶 KNO3
请根据实验和 KNO3 溶解度曲线回答下列问题(水的密度以 1g/mL 计):
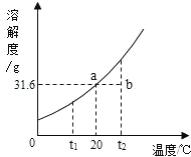
实验操作 | 实验结果 |
取 100mL 水,加入 25g KNO3,搅拌,20℃ | 全部溶解,得溶液① |
再加 Xg KNO3,搅拌,20℃ | 恰好饱和,得溶液② |
再加 25g KNO3,搅拌,20℃ | 得溶液③ |
加热 | 全部溶解,得溶液④ |
冷却至 20℃ | 晶体析出,得溶液⑤ |
(4)溶液③的质量为_____;一定属于不饱和溶液的是(填数字序号)_____; 溶质的质量分数一定相等的是(填序号)_____.
(5)析出晶体的质量为(填序号)_____.
A.25g B.X+25g C.X+100g.
【答案】CBA .BCD .DFG .131.6g ;① ;②③ .A .
【解析】
(1)根据提纯的基本操作步骤包括溶解-过滤-蒸发分析;(2)A、根据过滤时滤纸有破损造成食盐有一部分进入滤液没有被蒸发分析;B、根据蒸发时有固体溅出导致原混合物中的食盐没有全部转化成产品分析;C、根据把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上,导致称量时质量减小分析;D、根据溶解11g含有泥沙的NaCl时,加入的水量不足导致食盐有一部分没被溶解分析。(3)根据配制溶液的步骤选择仪器;(4)根据溶解度分析饱和溶液与不饱和溶液以及溶质质量分数;(5)根据溶解度定义分析析出晶体的质量。
(1)提纯的基本操作步骤包括溶解-过滤-蒸发,从流程图可知操作①、②、③依次为图中的CBA;(2)A、过滤时滤纸有破损造成含泥沙的食盐有一部分进入滤液,被蒸发结晶析出导致产量偏高,错误;B、蒸发时有固体溅出导致原混合物中的食盐没有全部转到产品中,从而导致产率偏低,正确;C、把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上,导致称量时质量减小,从而导致产率偏低,正确;D、溶解11g含有泥沙的NaCl时,加入的水量不足导致食盐有一部分没被溶解,从而使食盐没有全部转化为产品,从而导致产率偏低,正确。故选BCD;(3)配制氯化钠溶液的步骤是计算、称量、量取、溶解,因此不需要用到的仪器有漏斗、蒸发皿、酒精灯。故选DFG;(4)根据溶解度曲线可知20℃时硝酸钾的溶解度为31.6g,因此取100mL水,加入25gKNO3,搅拌得到的溶液①是不饱和溶液,再加XgKNO3,搅拌得到的②溶液恰好饱和,因此X的值为6.6g,再加25g硝酸钾此时不能再溶解,因此得到的溶液③为饱和溶液且有25g固体剩余,②③的溶质质量分数相同,加热后固体全部溶解,得到的溶液④可能刚好饱和也可能不饱和;再冷却到20℃时硝酸钾析出25g。故溶液③的质量为131.6g;一定属于不饱和溶液的是 ①;溶质的质量分数一定相等的是(填序号) ②③;(5)析出晶体的质量为25g,选A。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案【题目】小丽去爷爷家,发现爷爷买了一台氧立得便携式制氧器,她仔细阅读了所用制氧剂的说明对制氧剂产生了兴趣。


(提出问题)A剂的主要成分和B剂的作用各是什么
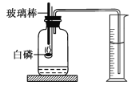
(查阅资料)过碳酸钠(化学式2Na2CO3·3H2O2)俗称固体双氧水,白色颗粒。过碳酸钠溶于水时,分解生成碳酸钠(Na2CO3)和过氧化氢,是很好的固体氧释放剂。
碳酸钠能溶于水,能和稀盐酸反应,放出二氧化碳。
(做出猜想)
猜想Ⅰ:A剂可能是过碳酸钠。
猜想Ⅱ:B剂的作用可能是催化作用。
(设计实验) 请你帮助小丽完成下列实验报告。
验证猜想 Ⅰ
主要操作步骤 | 主要实验现象 | 实验结论 | |
| 如左图,取少量A剂放入试管中,加水溶解,然后____ | 生成大量气泡 ________ | ___ |
实验② | 另取少量A剂放入试管中,加水溶解,然后将所得溶液倒入另一只装有少量二氧化锰的试管中。 稍后将带火星的木条放在试管口 | 生成大量气体 此气体使带火星的木条复燃 | _____ |
综合上述①、②的实验结果分析,得出初步结论:A剂的主要成分是过碳酸钠 | |||
验证猜想Ⅱ
实验步骤 | 实验现象 | 解释或结论 | |
实验③ | 将一包A剂和一包B剂放在盛有水的制氧仓中,制完氧之后,取出剩余物,过滤、洗涤、干燥、称重。 | 称得固体质量为3g | _______ |
实验④ | _______________ | 产生大量气体,该气体使带火星的木条复燃 | _________ |
综合上述③、④的实验结果分析,得出结论:B剂的作用是催化作用 | |||
(反思拓展)请你根据制氧剂的特点,提出保存的方法___________________________。
对反应后的剩余物的处理提一条合理化建议:_______________________________。
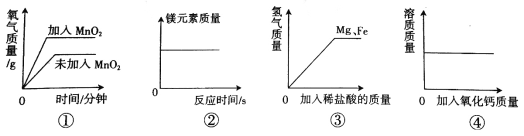
【题目】兴趣小组的同学们在老师的指导下进行实验室制取氧气的实验。
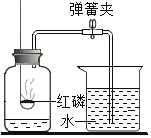
(1)甲同学称取一定质量的高锰酸钾固体放入大试管中,将温度控制在250℃加热制取O2。实验结束时,乙同学发现用排水法收集到的氧气大于理论产量。针对这一现象,进行了如下探究:
[提出猜想]猜想I:反应生成的二氧化锰分解放出氧气;猜想II:反应生成的锰酸钾分解放出氧气;猜想III:_________________
[实验验证]同学们分成两组,分别进行下列实验:第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想______错误;第二组同学取锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论。该组同学选择的实验方法是______________。
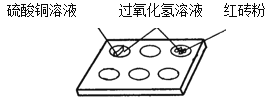
(2)白色点滴板是带有空穴的白色瓷板,可用作微型化学反应。在寻找新催化剂时,将一定量的红砖粉、硫酸铜溶液……分别加入点滴板中,再分别滴入过氧化氢溶液(如图所示),观察到过氧化氢溶液产生气泡的速率加快。据此现象得出结论:红砖粉、硫酸铜溶液等也能做过氧化氢溶液的催化剂。小红认为不正确,
理由一:未探究它们的质量在反应前后是否不变;
理由二:_______________________。
白色点滴板作为反应容器的优点有______________________
(3)通过对催化剂的实验探究,同学们还想探究影响反应速率的其他因素。于是在老师的指导下查阅资料,资料表明:影响反应速率的其他因素还有温度,浓度,物质的纯度和固体的形状大小等。根据查阅的资料同学们设计了实验室用锌与稀硫酸反应制取氢气的实验。反应过程中,用前 10 min 内收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表四组实验,获得数据如下表。
验实号编 | 试剂 | 前 10 min 内产生的氢气体积(mL) | |
不同纯度的锌 | 不同体积和浓度的稀硫酸 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
① 比较实验 a 和实验 b ,可以得到的结论是________________________。
② 为了研究硫酸浓度对反应快慢的影响,需比较实验_____和实验_____(填编号)。
③ 控制其他条件相同,需控制的条件是__________________(例举一种条件即可)。
通过实验,同学们明白了一个道理,物质的纯度对化学反应速率有很大影响,但是不一定是纯度越大反应速率越快,有时候也会有一些特殊情况。