题目内容
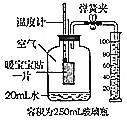
【题目】小沛用如图所示装置测量空气中氧气含量,集气瓶容积为700mL,集气瓶内水的体积为100mL,实验开始前量筒200mL,实验结束后量筒中水的体积为100mL。
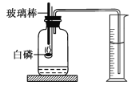
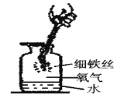
(1)用力将预先加热过的玻璃棒按下与白磷接触,观察到白磷燃烧时的现象是________________,整个实验过程中,量筒内水面的变化情况是________________。
(2)将步骤(1)后的集气瓶内气体换成等体积的混合气体(该混合气体中氧气体积分数为1%,氮气体积分数为99%),再次实验,发现白磷不能被点燃。由此可知,在所有操作均规范的情况下,步骤(2)实验所测得的空气中氧气的含量比理论_____(填“偏大”、“偏小”或“不变”),该实验测得氧气体积是_____mL。
(3)已知氧气密度为1.4g/L,每31g白磷燃烧需要消耗40g氧气,若操作中要尽量消耗完瓶中的氧气,求完成此实验至少需要白磷_________克。(结果保留两位小数)
【答案】冒出大量的白烟,放出热量; 先升高后降低. 偏小; 100. 0.11g,
【解析】
(1)白磷燃烧的现象是冒出大量的白烟,放出热量;整个实验过程中,开始时反应放热,瓶中气体压强增大,导致瓶中部分水进入量筒中,量筒中液面升高,反应结束后,冷却至室温,气体压强减小,又由于瓶中氧气被消耗,因此量筒中的水进入瓶中,故量筒内水面的变化情况是先升高后降低。
(2)将步骤(2)后的集气瓶内气体换成等体积的混合气体(该混合气体中氧气体积分数为1%,氮气体积分数为99%),再次实验,发现白磷不能被点燃,即使白磷过量,也不能把瓶中氧气完全消耗,由此可知,在所有操作均规范的情况下,步骤(2)实验所测得的空气中氧气的含量比理论值偏小;由于实验结束后量筒中水的体积为100mL,即量筒中的水减少了100mL,说明瓶中氧气的体积是100mL,因此该实验测得氧气体积是100mL。
(4)100ml氧气的质量为0.1L×1.4g/L=0.14g,消耗0.014g氧气需要白磷的质量为![]() ×0.014g=0.11g
×0.014g=0.11g
答:若操作中要尽量消耗完瓶中的氧气,完成此实验至少需要0.11g白磷.

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案【题目】某兴趣小组做了如下实验.
(实验一)提纯 NaCl
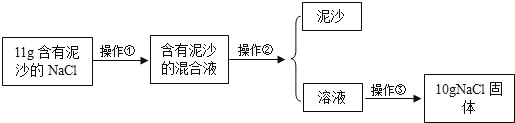
请根据实验回答下列问题:
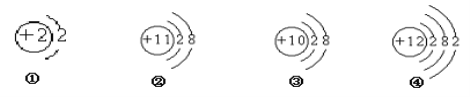
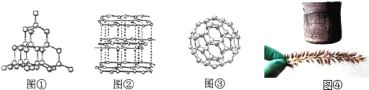
(1)操作①、②、③依次为图中的(填序号)______.
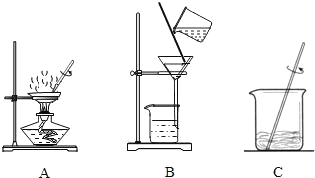
(2)若得到 NaCl 的产率比实际值偏低,则可能的原因是(填序号)_______.
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上
D.溶解 11g 含有泥沙的 NaCl 时,加入的水量不足
(3)用上述实验所得的氯化钠配制溶质质量分数为 5%的氯化钠溶液 50g,不需 要的仪器为(填序号)_____.
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒 精灯
(实验二)溶解和结晶 KNO3
请根据实验和 KNO3 溶解度曲线回答下列问题(水的密度以 1g/mL 计):
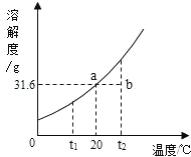
实验操作 | 实验结果 |
取 100mL 水,加入 25g KNO3,搅拌,20℃ | 全部溶解,得溶液① |
再加 Xg KNO3,搅拌,20℃ | 恰好饱和,得溶液② |
再加 25g KNO3,搅拌,20℃ | 得溶液③ |
加热 | 全部溶解,得溶液④ |
冷却至 20℃ | 晶体析出,得溶液⑤ |
(4)溶液③的质量为_____;一定属于不饱和溶液的是(填数字序号)_____; 溶质的质量分数一定相等的是(填序号)_____.
(5)析出晶体的质量为(填序号)_____.
A.25g B.X+25g C.X+100g.