题目内容
【题目】小丽去爷爷家,发现爷爷买了一台氧立得便携式制氧器,她仔细阅读了所用制氧剂的说明对制氧剂产生了兴趣。


(提出问题)A剂的主要成分和B剂的作用各是什么
(查阅资料)过碳酸钠(化学式2Na2CO3·3H2O2)俗称固体双氧水,白色颗粒。过碳酸钠溶于水时,分解生成碳酸钠(Na2CO3)和过氧化氢,是很好的固体氧释放剂。
碳酸钠能溶于水,能和稀盐酸反应,放出二氧化碳。
(做出猜想)
猜想Ⅰ:A剂可能是过碳酸钠。
猜想Ⅱ:B剂的作用可能是催化作用。
(设计实验) 请你帮助小丽完成下列实验报告。
验证猜想 Ⅰ
主要操作步骤 | 主要实验现象 | 实验结论 | |
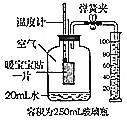
| 如左图,取少量A剂放入试管中,加水溶解,然后____ | 生成大量气泡 ________ | ___ |
实验② | 另取少量A剂放入试管中,加水溶解,然后将所得溶液倒入另一只装有少量二氧化锰的试管中。 稍后将带火星的木条放在试管口 | 生成大量气体 此气体使带火星的木条复燃 | _____ |
综合上述①、②的实验结果分析,得出初步结论:A剂的主要成分是过碳酸钠 | |||
验证猜想Ⅱ
实验步骤 | 实验现象 | 解释或结论 | |
实验③ | 将一包A剂和一包B剂放在盛有水的制氧仓中,制完氧之后,取出剩余物,过滤、洗涤、干燥、称重。 | 称得固体质量为3g | _______ |
实验④ | _______________ | 产生大量气体,该气体使带火星的木条复燃 | _________ |
综合上述③、④的实验结果分析,得出结论:B剂的作用是催化作用 | |||
(反思拓展)请你根据制氧剂的特点,提出保存的方法___________________________。
对反应后的剩余物的处理提一条合理化建议:_______________________________。
【答案】滴加稀盐酸,将气体通入澄清石灰水中澄清石灰水变混浊A剂溶于水有Na2CO3生成A剂溶于水有过氧化氢生成B剂在制氧前后质量不变另取少量A剂放入试管中,加足量水溶解,再加入实验③所得干燥固体,然后将带火星的木条伸入试管B剂在制氧前后化学性质不变应放在干燥、阴凉处所得残余物过滤,固体可重复使用,液体蒸干可得纯碱
【解析】
(设计实验)实验①:根据后面的实验现象可知,固体溶于水形成溶液后,经过某种操作生成了二氧化碳,根据已知固体有可能是碳酸钠可知,此时需要加入盐酸;实验②:根据操作以及现象可以判定,固体溶于水产生使带火星木条复燃的气体(氧气),说明A剂溶于水产生氧气;故填:⑴滴加稀盐酸,将气体通入澄清石灰水中;澄清石灰水变混浊;A剂溶于水有Na2CO3生成; A剂溶于水有过氧化氢生成;B剂在制氧前后质量不变;另取少量A剂放入试管中,加足量水溶解,再加入实验③所得干燥固体,然后将带火星的木条伸入试管;B剂在制氧前后化学性质不变;
(反思拓展)根据过碳酸钠溶于水或受热时会发生分解,可建议制氧剂应放置于干燥、阴凉处;根据探究,制氧后B剂性质及化学性质不变,可建议重复使用;根据探究实验,制氧后的溶液为碳酸钠溶液,可建议蒸干溶液获得纯碱;故答案为:放在干燥、阴凉处;所得残余物过滤,固体可重复使用,液体蒸干可得纯碱.

【题目】某兴趣小组做了如下实验.
(实验一)提纯 NaCl
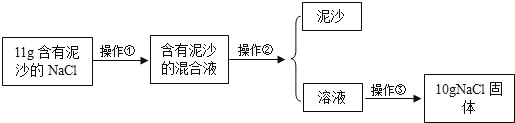
请根据实验回答下列问题:
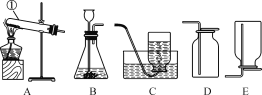
(1)操作①、②、③依次为图中的(填序号)______.
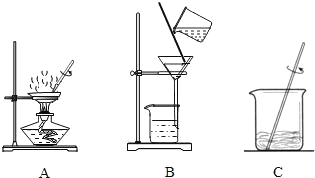
(2)若得到 NaCl 的产率比实际值偏低,则可能的原因是(填序号)_______.
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.把晶体从蒸发皿转移到天平上称量时,有少量粘在了蒸发皿上
D.溶解 11g 含有泥沙的 NaCl 时,加入的水量不足
(3)用上述实验所得的氯化钠配制溶质质量分数为 5%的氯化钠溶液 50g,不需 要的仪器为(填序号)_____.
A.量筒 B.天平 C.烧杯 D.漏斗 E.蒸发皿 F.玻璃棒 G.酒 精灯
(实验二)溶解和结晶 KNO3
请根据实验和 KNO3 溶解度曲线回答下列问题(水的密度以 1g/mL 计):
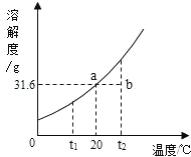
实验操作 | 实验结果 |
取 100mL 水,加入 25g KNO3,搅拌,20℃ | 全部溶解,得溶液① |
再加 Xg KNO3,搅拌,20℃ | 恰好饱和,得溶液② |
再加 25g KNO3,搅拌,20℃ | 得溶液③ |
加热 | 全部溶解,得溶液④ |
冷却至 20℃ | 晶体析出,得溶液⑤ |
(4)溶液③的质量为_____;一定属于不饱和溶液的是(填数字序号)_____; 溶质的质量分数一定相等的是(填序号)_____.
(5)析出晶体的质量为(填序号)_____.
A.25g B.X+25g C.X+100g.
【题目】某化学兴趣小组同学在回收废旧电池的同时,开展了如下的实验探究。
(查阅资料)废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。
(实验1)废干电池的拆卸与处理
(1)兴趣小组同学将废旧干电池卸下的锌筒、碳棒冲洗干净,备用。
(2)将铜帽放入盐酸中,除去锈污,冲洗备用。
(实验2)检验废干电池筒内黑色固体中的二氧化锰存在
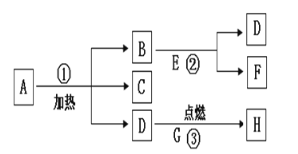
兴趣小组同学设计了如下图所示的实验:
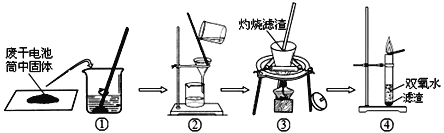
(1)操作③灼烧黑色滤渣时,会产生一种气体能使澄清石灰水变浑浊,灼烧时的表达式为____;澄清石灰水变浑浊的表达式为____。
(2)操作④试管中产生的气体能使带火星木条复燃,该气体为__________。
(3)由此得出结论:滤渣中黑色固体化学式为_____和 _____
(实验3)利用回收锌皮制取氢气及相关探究
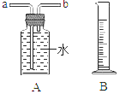
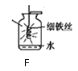
(1)用锌皮和稀硫酸制取氢气。用适当的发生装置,采用排水法收集并测定氢气的体积(如右图),气体从装置A导管口___(填“ a ”或“ b ” ) 进,选用仪器B测量排出水的体积,仪器B名称是______。
(2)探究影响锌与稀硫酸反应快慢的因素。反应过程中用前10 min 内
收集的氢气体积比较反应的快慢。控制其他条件相同,进行下表4组实验,获得数据如下。
实验编号 | 试剂 | 前10 min内产生的 氢气体积(mL) | |
锌的纯度 | 稀硫酸的体积和浓度 | ||
a | 纯锌 | 30 mL 30 % | 564.3 |
b | 含杂质的锌 | 30 mL 30 % | 634.7 |
c | 纯锌 | 30 mL 20 % | 449.3 |
d | 纯锌 | 40 mL 30 % | 602.8 |
[数据分析]
①比较实验a和实验b得到的结论是:_________________________。
②为了研究硫酸浓度对反应快慢的影响,需比较实验____________(填实验编号)。
③探究影响该反应快慢的因素,还需控制的条件是:______________(一例即可)。
(实验4)探究经处理干净的二氧化锰在氯酸钾分解反应中的催化作用(已知氯化钾可溶)
(1)把干燥纯净的24.5g氯酸钾和5.5g二氧化锰混匀、装入大试管中,加热。
(2)待反应完全后,将试管冷却、称量,得到20.4g残留固体。
(3)再将残留固体经溶解、_____、洗涤、干燥、称量,得到5.5g黑色固体。
[数据分析]
①该实验说明:二氧化锰在氯酸钾分解反应前后,_____不变。
②完全反应后制得氧气的质量是______g。(提示:已知所有化学反应遵循如下规律:参加化学反应的各物质的质量总和等于反应后生成各生成物的质量总和)
[实验反思]
要证明二氧化锰是氯酸钾分解反应的催化剂,还要做一个对比实验:将等质量的2份氯酸钾粉末,其中一份加入少量的上述实验所得二氧化锰混匀、装入试管,另一份装入另一试管,加热,比较____________的大小。