��Ŀ����
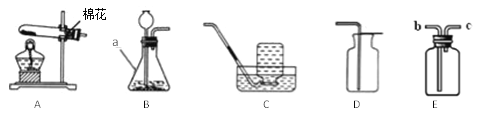
����Ŀ����ϰ���ϣ���ʦ������ƿû�б�ǩ�İ�ɫ���壬�ֱ���̼���ơ��������ơ��Ȼ�狀��Ȼ��ƣ�Ҫ��ͬѧ�����ʵ�鷽�����м���С���������ͼ��ʾ�ķ���������ʵ�飨ʵ�������ÿһ�����ȡ��ԭ�������ʣ���
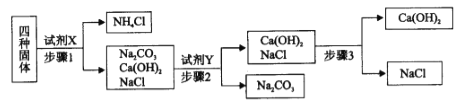
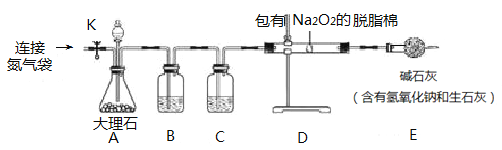
(1)�������Լ�X����ʯ�ң���ʯ�����Ȼ�炙�ϵ�ʵ��������____________________��д����ʯ����NH4C1��Ӧ�Ļ�ѧ����ʽ___________________________��
(2)�����Լ�Y������ʵ������ȡCO2����Y�Ļ�ѧʽ��____���Լ�Y�뱻����������ʷ�Ӧ�Ļ�ѧ����ʽΪ________��
(3)����3�зֱ�ȡ���������ֹ�������ˮ������Һ��pH���������������ʣ���pH��ֽ����ҺpH�IJ����ǣ�ȡһСƬpH��ֽ���ڲ���Ƭ�ϣ�_____________________________������pH��ֵ��
���𰸡� �����д̼�����ζ�����壻 2NH4Cl+Ca��OH��2=CaCl2+2H2O+2NH3�� HCl�� Na2CO3 + 2HCl == 2NaCl + H2O + CO2���� �øɾ��IJ�����պȡ������Һ������pH��ֽ��һ����,��ɫ�����ֽ��ʾ����ɫ�����ɫ�����ա�
����������1���Ȼ�������������ƻ�Ϸ�Ӧ���ɰ������д̼�����ζ����ʯ����NH4Cl��Ӧ�Ļ�ѧ����ʽΪ��2NH4Cl+Ca��OH��2=CaCl2+2H2O+2NH3������2��ʵ���ҳ���ʯ��ʯ����Ҫ�ɷ���̼��ƣ���ϡ���ᷴӦ��ȡCO2��̼��ƺ�̼���ơ��������ơ��Ȼ��ƶ�����Ӧ���������̼�ᷴӦ���ɶ�����̼���壬�������ݶ���̼���Ƽ����������Y�Ļ�ѧʽ��HCl�������뱻̼���Ʒ�Ӧ���ɶ�����̼���Ȼ��ơ�ˮ����Ӧ�Ļ�ѧ����ʽΪNa2CO3 + 2HCl == 2NaCl + H2O + CO2����(3)��pH��ֽ����ҺpH�IJ����ǣ�ȡһСƬpH��ֽ���ڲ���Ƭ�ϣ��øɾ��IJ�����պȡ������Һ������pH��ֽ��һ����,��ɫ�����ֽ��ʾ����ɫ�����ɫ������,������ͬ��ɫ��pHֵ��

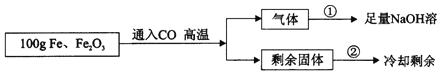
����Ŀ���ס��ҡ����������ʵ�ת����ϵ����ͼ��ʾ����������ʾ��Ӧһ��ʵ�֣��������ʺͷ�Ӧ��������ȥ��������ѡ���ʵ��ͼʾת������
ѡ�� | �� | �� | �� |
A | H2SO4 | H2 | H2O |
B | C | CO | CO2 |
C | Ca(OH)2 | CaCl2 | CaCO3 |
D | NaOH | NaCl | NaNO3 |
A. A B. B C. C D. D
����Ŀ��С��ȡ����п�̸ɵ�ؽ���̽���������ֵ���ڲ��ṹ��ͼ1��ʾ��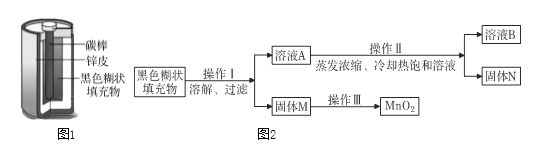
���������ϡ�(1)пƤΪ����п(������������)
(2)��ɫ��״�������̿�ڡ�MnO2��ZnC12��NH4Cl�����
(3)�й����ݼ��±�
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ��/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
��ʵ��̽��һ��С��ȡ������ɫ��״������ͼ2��ʾʵ�����̽���̽����
(1)��ҺA��������Ҫ��______(�ѧʽ)���������в�����ȴ�ȱ�����Һ�ķ���ʵ�����߷����������____________��
(2)���ӹ���M �еõ��ϴ���MnO2��������ɲ��õļ�㷽����____________��
��ʵ��̽������С��ȡ������пƤ����ɰֽ��ĥ�ɾ�������С�飬����ʵ�顣
(1)ȡһ��пƤ����ʢ������ϡ������ձ��У���ZnCl2���ɡ�
�� ʵ���пɹ۲쵽��������_________��
�� ���и������ʻ�Ϻ�Ҳ������ZnCl2����_________(����ĸ���)��
A��ZnO��ϡ���� B��ZnSO4��Һ��BaC12��Һ
C��ZnCO3��NaCl��Һ D��Zn(NO3)2��Һ��NH4Cl��Һ
(2)��ȡһ��пƤ����ʢ��һ����CuSO4��Һ���ձ��У���ַ�Ӧ��õ���ҺE����F������ҺE��ֻ��һ������ʱ����������________(�ѧʽ)��������F��ֻ��һ������ʱ����ҺE�����ٺ���________�����ʡ�
������6.5gпƤ������ϡ������ȫ��Ӧ������������������________0.2g(ѡ�<������>����=��)��