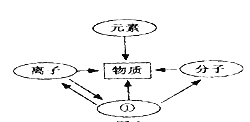
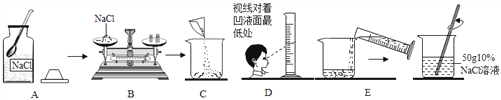
题目内容
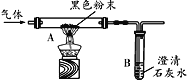
【题目】小明取酸性锌锰干电池进行探究,他发现电池内部结构如图1所示。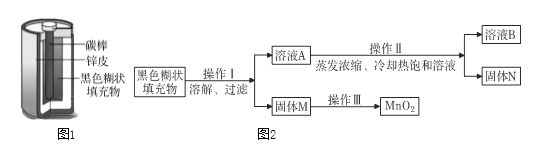
【查阅资料】(1)锌皮为金属锌(含有少量的铁)
(2)黑色糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
(3)有关数据见下表
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
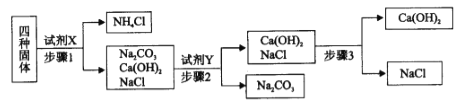
【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。
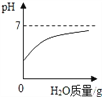
(1)溶液A中溶质主要有______(填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是____________。
(2)欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是____________。
【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
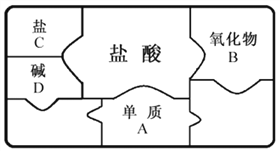
(1)取一块锌皮放入盛有适量稀盐酸的烧杯中,有ZnCl2生成。
① 实验中可观察到的现象是_________;
② 下列各组物质混合后,也能生成ZnCl2的有_________(填字母序号)。
A.ZnO与稀盐酸 B.ZnSO4溶液与BaC12溶液
C.ZnCO3与NaCl溶液 D.Zn(NO3)2溶液与NH4Cl溶液
(2)另取一块锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含一种溶质时,该溶质是________(填化学式);当固体F中只含一种物质时,溶液E中最少含有________种溶质。
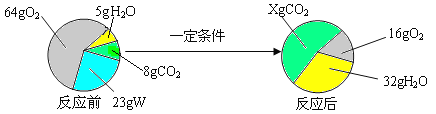
③若将6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量________0.2g(选填“<”、“>”或“=”)。
【答案】 NH4Cl、ZnCl2 两者的溶解度受温度变化的影响不同; 灼烧(在空气中充分燃烧); 固体溶解,有大量气泡产生;; A、B ZnSO4; 2; >。
【解析】(1)黑色糊状填充物中的NH4Cl、ZnCl2易溶于水,溶液A中溶质主要有NH4Cl、ZnCl2;操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是两者的溶解度受温度变化的影响不同;(2)在空气中充分燃烧,碳转化成二氧化碳逸散到空气中,以除去炭黑;【实验探究二】(1)①锌与盐酸反应生成氢气,可观察到有气泡产生;属于由一种单质和一种化合物生成另一种单质和另一种化合物的置换反应;②A.ZnO+2HCl=ZnCl2+H2O,正确;B.ZnSO4+BaC12==BaSO4↓+ZnCl2,正确;C.ZnCO3与NaCl溶液不反应,错误;D.Zn(NO3)2溶液与NH4Cl溶液不反应,错误。故选AB。(2)Zn+CuSO4=ZnSO4+Cu,Fe+CuSO4=FeSO4+Cu,金属活动性顺序相差大的之间先反应,故Zn+CuSO4=ZnSO4+Cu先反应。当溶液E中只含一种溶质时,该溶质是ZnSO4,当固体F中只含一种物质时,该固体物质是铜,溶液E中最少含有ZnSO4、FeSO4两种溶质。③6.5g纯净的锌与足量稀硫酸反应,生成0.2g氢气,等质量的锌、铁与酸反应,铁生成氢气多,将含有铁的6.5g锌皮与足量稀硫酸完全反应,生成氢气的质量>0.2g。