题目内容
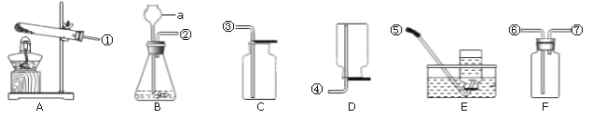
【题目】小安同学用加热氯酸钾和二氧化锰的方法来制取氧气,当收集满一瓶氧气体后,停止加热。小安对试管中的剩余固体的成分做了如下猜想:①是氯酸钾;②是氯化钾;③是氯化钾和二氧化锰。
(1)经过同学们讨论,认为三种猜想中一定不成立的是______(填番号)。还有一种可能性,请你来完成,作一个合理的猜想,试管中的剩余固体可能是__________。
(2)若你的猜想正确,请完成你的证明实验。
实验方案 | 实验现象 | 实验结论 |
将试管内的物质继续加热,并用___________ | _____________ | 你的猜想正确 |
(3)已知二氧化锰不溶于水,氯酸钾和氯化钾易溶于水。实验完毕后,小安同学想回收二氧化锰。其具体操作是:先将剩余固体放入烧杯中,加水充分溶解,然后过滤、洗涤、_______、最后再称量,发现它的质量与反应前 _________(填“有”或“没有”)发生变化。
(4)该反应中二氧化锰在反应前后固体混合物中的质量分数将______ (填“变大”、“变小”或“不变”)。
(5)写出该反应的化学符号表达式 ________。
【答案】①② 氯酸钾、氯化钾、二氧化锰(或KClO3、KCl、MnO2) 带火星的木条伸到(入)试管口 木条复燃 干燥 (或烘干) 没有 变大 KClO3![]() KCl+O2
KCl+O2
【解析】
(1)氯酸钾受热分解生成氯化钾和氧气,所以剩余固体中一定含有氯化钾;由于催化剂在反应前后的质量和化学性质都不变,所以剩余固体中一定含有二氧化锰;如果没有反应完全,生成物中有KClO3、KCl、MnO2;
(2)由于氯酸钾在二氧化锰作催化剂的条件下完全分解,生成氯化钾和氧气,氧气可使带火星小木条复燃,据此设计实验;
(3)二氧化锰不溶于水,锰酸钾易溶于水,所以可采取过滤的方法提取二氧化锰,先溶解固体,再过滤,然后将固体洗涤并烘干即可;二氧化锰作为催化剂,质量不变;
(4)二氧化锰作为催化剂,质量不变,而氯酸钾分解,剩余固体的质量不断减少一直到完全反应,所以在对试管加热过程中,固体混合物中二氧化锰的质量分数变大;
(5)氯酸钾在二氧化锰作催化剂的条件下完全分解,生成氯化钾和氧气,反应的化学符号表达式:KClO3![]() KCl+O2。
KCl+O2。

 应用题作业本系列答案
应用题作业本系列答案