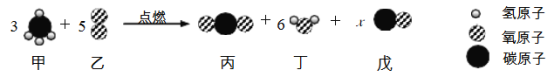题目内容
【题目】在氯酸钾受热分解的反应中,二氧化锰的催化问题到目前为止还没有比较明确的解释。鉴于制得的氧气 中含有氯气(Cl2)的气味,生成的白色固体氯化钾中又略显紫色,有人认为反应过程如下(①以下化学方程都已配平②字母 A、B、C、D 分别表示四种不同的物质):
①2KClO3+2MnO2![]() 2A+B↑+C↑
2A+B↑+C↑
②2A ![]() D+MnO2+C↑
D+MnO2+C↑
③B+D ![]() 2KCl+MnO2+C↑
2KCl+MnO2+C↑
(1)请写出 C 的化学式:___;
(2)写出③的化学方程式:___。
【答案】O2 Cl2 K2MnO4 ![]() 2KCl MnO2 O2
2KCl MnO2 O2
【解析】
由于生成的气体既有氧气又有氯气,根据化学反应前后元素的种类和个数不变可知,由于反应方程式均已配平,所以A的化学式中必含有1个钾原子,1个锰原子,由于生成的气体既有氧气又有氯气,所以B、C其中一种是氧气,另一种是氯气,分析③反应的情况结合实验室用高锰酸钾制取氧气的化学方程式为:2KMnO4![]() K2MnO4 + MnO2 + O2↑;可知C为氧气,B应为氯气,所以可知A的化学式中还应有4个氧原子,即A是KMnO4,B是Cl2,C是O2,D是K2MnO4。
K2MnO4 + MnO2 + O2↑;可知C为氧气,B应为氯气,所以可知A的化学式中还应有4个氧原子,即A是KMnO4,B是Cl2,C是O2,D是K2MnO4。
根据以上分析可知:
(1)C是氧气,的化学式为:O2;
(2)③的化学方程式:Cl2 K2MnO4 ![]() 2KCl MnO2 O2 。
2KCl MnO2 O2 。

【题目】如图所示,在小烧杯A中装入30 mL蒸馏水,再滴入3滴酚酞,在小烧杯B中装入30 mL浓氨水,用一大烧杯把A、B两个烧杯罩在一起,过一段时间看到的现象是__,该实验说明___。
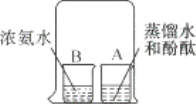
一些同学对上述结论有不同看法,主要有以下两种猜测:
第一种:B烧杯中的蒸馏水使酚酞试液变红;
第二种:B烧杯中浓氨水挥发出氨气,扩散到A烧杯中的溶液中使酚酞试液变红。
①你认为____猜测正确,②为证明这两种猜测,现设计如下的实验(请完成下表):
实验内容、方法 | 现象 | 结论 |
用洁净的小烧杯取20 mL蒸馏水,滴入2~3滴酚酞试液,观察现象 | 不变色 | 水___使酚酞变色(填“能”或“不能”,下同) |
取一张滤纸,滴入酚酞试液,待晾干后,放在装有浓氨水的试剂瓶上方 | 酚酞不变色 | 氨气____使酚酞变色 |
将少量氨气通入含有酚酞试液的蒸馏水中 | 溶液变成 ___色 | 氨气溶解在水中形成的氨水能使酚酞变色 |
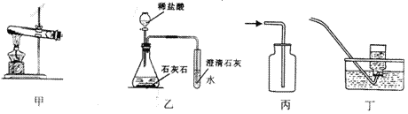
【题目】小安同学用加热氯酸钾和二氧化锰的方法来制取氧气,当收集满一瓶氧气体后,停止加热。小安对试管中的剩余固体的成分做了如下猜想:①是氯酸钾;②是氯化钾;③是氯化钾和二氧化锰。
(1)经过同学们讨论,认为三种猜想中一定不成立的是______(填番号)。还有一种可能性,请你来完成,作一个合理的猜想,试管中的剩余固体可能是__________。
(2)若你的猜想正确,请完成你的证明实验。
实验方案 | 实验现象 | 实验结论 |
将试管内的物质继续加热,并用___________ | _____________ | 你的猜想正确 |
(3)已知二氧化锰不溶于水,氯酸钾和氯化钾易溶于水。实验完毕后,小安同学想回收二氧化锰。其具体操作是:先将剩余固体放入烧杯中,加水充分溶解,然后过滤、洗涤、_______、最后再称量,发现它的质量与反应前 _________(填“有”或“没有”)发生变化。
(4)该反应中二氧化锰在反应前后固体混合物中的质量分数将______ (填“变大”、“变小”或“不变”)。
(5)写出该反应的化学符号表达式 ________。