题目内容
【题目】下列实验设计能够达到对应实验目的的是
选项 | 实验目的 | 实验设计 | 选项 | 实验目的 | 实验设计 |
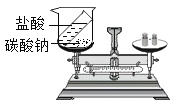
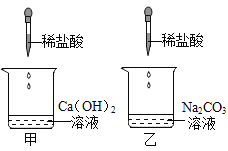
A | 验证质量守恒定律 |
| B | 证明二氧化碳气体的密度大于空气 |
|
C | 证明分子是不断运动的 |
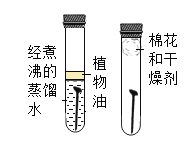
| D | 探究铁钉锈蚀的条件 |
|
A.AB.BC.CD.D
【答案】B
【解析】
A、碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水,二氧化碳逸出,不能用来验证质量守恒定律,不符合题意;
B、将二氧化碳倒入烧杯中,下层蜡烛先熄灭,说明二氧化碳不燃烧,也不支持燃烧,且二氧化碳的密度比空气大,可以达到实验目的,符合题意;
C、浓盐酸具有挥发性,挥发出的氯化氢气体与水结合生成盐酸,盐酸显酸性,不能使无色酚酞试液变色,无明显现象,不能证明分子是不断运动的,不符合题意;
D、左边试管中的铁钉与水接触,与氧气不接触,不能生锈,右边试管中的铁钉与空气接触,与水不接触,不能生锈,两个铁钉都不能生锈,不能用来探究铁钉锈蚀的条件,不符合题意。
故选B。

【题目】小明同学在练习“金属的化学性质”实验操作时,发现几支试管中气泡产生的速率有快有慢,于是他与小芳同学一起合作进行如下探究。
(提出问题)金属与酸反应的快慢受哪些因素影响呢?
(猜想与假设)猜想一:可能与酸的浓度有关;
猜想二:可能与金属的种类有关;
猜想三:可能与金属的形状有关。
(设计并进行实验 )为了验证猜想,小明和小芳设计下图所示装置进行实验。
编号 | 盐酸的浓度(均取20 mL) | 金属(均取2g) | 金属的形状 | 收集50 mL氢气所需时间/s |
① | 10% | 铝 | 粉状 | 70 |
② | 10% | 铁 | 片状 | 120 |
③ | 10% | 铝 | 片状 | 112 |
④ | 20% | 铁 | 片状 | 110 |
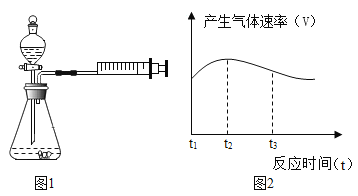
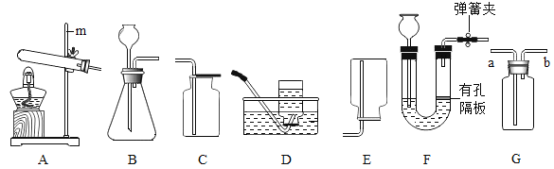
(1)小明和小芳检查图1装置气密性的方法是:关闭分液漏斗活塞,用力将注射器活塞向右移动一 段距离,停止用力后松手,若观察到_________________,则表示气密性良好。
(2)写出铝与盐酸反应的化学方程式:____________________________________。
(收集证据)
(3)要比较金属的形状对反应快慢的影响,应选择的实验编号是________________________。
(得出结论)
(4)通过上述四个实验,你得出的影响金属与酸反应的快慢因素有________________________。
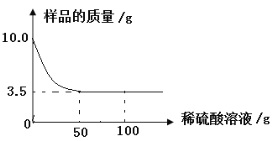
(5)实验①中试管外壁发烫,说明铝与盐酸的反应是放热反应,实验测得该反应中产生气体的速率(v)与时间(t)的关系如图2所示,你认为在t2~t3时间段内反应速率逐渐减慢的主要原因是____________________。
(实验拓展)
(6)小明将盐酸换成稀硫酸继续进行实验,发现铝粉和稀硫酸的反应现象不明显。为什么铝粉易与盐酸反应而难与稀硫酸反应呢?小明认为可能是Cl-的存在使酸和铝的反应容易进行。请你帮助小明设计一个合理的实验来验证假设:___________。