题目内容
【题目】将12.5g石灰石样品放到烧杯中,加入100g稀盐酸恰好反应,烧杯内剩余物质总质量为108.1g。
请计算(1)生成的CO2质量 _______ g.
(2)所得溶液溶质的质量分数?_______(解题过程)(结果保留0.1%)
【答案】4.4 10.5%
【解析】
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量和反应生成的氯化钙的质量,进一步可以计算反应后所得溶液中溶质的质量分数。
解:(1)反应生成二氧化碳的质量为:12.5g+100g-108.1g=4.4g;
(2)设碳酸钙的质量为x,生成氯化钙的质量为y,
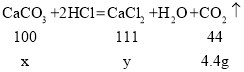
![]() x=10g,
x=10g,
![]() y=11.1g,
y=11.1g,
反应后所得溶液中溶质的质量分数为:![]() ×100%=10.5%。
×100%=10.5%。

练习册系列答案
相关题目