题目内容
【题目】化学活动小组在联欢会上表演了一个精彩的小魔术:向“矿泉水”中依次倾倒A、B、C三种溶液,出现如图所示的一系列变化,请运用初中化学的知识将魔术揭秘。
提示:“矿泉水”指代无色溶液;“牛奶”指代白色浑浊液体;“雪碧”指代反应中有气泡生成的无色溶液;“西瓜汁”指代红色溶液。
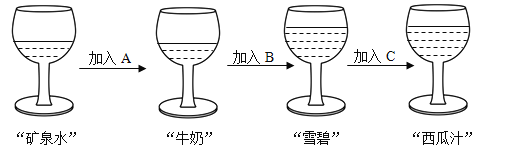
(1)“矿泉水”A、B、C中均只有一种溶质,“矿泉水”中溶质含钠元素,A中溶质由三种元素组成。推断“矿泉水”A、C中溶质分别为_____、_____、_____。
(2)在“牛奶”变“雪碧”的过程中,最多发生_____个化学反应;反应结束后,“雪碧”中溶质的成分是_____。
(3)将“矿泉水”中的溶质换成不含钠元素的其他类别物质,A、B、C不限,也能完成此魔术,则“矿泉水”和A中的溶质还可以是_____。
【答案】Ca(OH)2 Na2CO3 紫色石蕊 3 NaCl、CaCl2、HCl Ca(OH)2、Na2CO3
【解析】
(1)根据“矿泉水”A、B、C中均只有一种溶质,“矿泉水”中溶质含钠元素,A中溶质由三种元素组成,所以“矿泉水”是氢氧化钙,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀,所以A是碳酸钠,B稀盐酸,C是氢氧化钙,紫色石蕊遇酸变红色进行分析;
(2)根据碳酸钙与稀盐酸反应生成二氧化碳气体,故“牛奶”中加入B,有大量气泡产生,变成雪碧,则B物质是HCl,而稀盐酸可能与过量的氢氧化钙反应,或稀盐酸与过量的碳酸钠反应进行分析;
(3)根据碳酸根离子和钙离子反应会生成碳酸钙沉淀进行分析。
解:(1)“矿泉水”A、B、C中均只有一种溶质,“矿泉水”中溶质含钠元素,A中溶质由三种元素组成,所以“矿泉水”是氢氧化钙,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀,所以A是碳酸钠,B稀盐酸,C是氢氧化钙,紫色石蕊遇酸变红色,所以推断“矿泉水”A、C中溶质分别为:Ca(OH)2、Na2CO3、紫色石蕊;
(2)碳酸钙与稀盐酸反应生成二氧化碳气体,故“牛奶”中加入B,有大量气泡产生,变成雪碧,则B物质是HCl,而稀盐酸可能与过量的氢氧化钙反应,或稀盐酸与过量的碳酸钠反应,所以该过程发生的化学反应最多有3个,紫色石蕊溶液遇酸性溶液变为红色,C是一种紫色的溶液,则为紫色石蕊溶液,滴入“雪碧”中变为红色,所以雪碧的组成是NaCl、CaCl2、HCl;
(3)碳酸根离子和钙离子反应会生成碳酸钙沉淀,所以将“矿泉水”中的溶质换成不含钠元素的其他类别物质,A、B、C不限,也能完成此魔术,则“矿泉水”和A中的溶质还可以是:Ca(OH)2、Na2CO3。
故答案为:(1)Ca(OH)2、Na2CO3、紫色石蕊;(2)3,NaCl、CaCl2、HCl;(3)Ca(OH)2、Na2CO3。

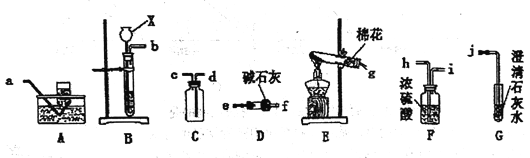
【题目】同学们为了探究氢氧化钙的化学性质,做了如下实验:
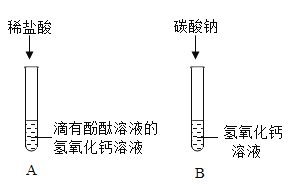
(1)试管A中观察到_____现象时,可证明氢氧化钙溶液与稀盐酸发生了反应。
(2)试管B中发生反应的化学方程式为_____;
(3)实验结束后,二支试管中的液体均为无色。同学们将二支试管中的无色液体倒入同一个洁净的烧杯中,静置一段时间,观察到烧杯底部有白色沉淀,上层溶液为无色。
[提出问题]无色溶液中除酚酞外还有哪些溶质?
[进行猜想]甲同学的猜想:NaCl
乙同学的猜想:NaCl、HCl
分析讨论]①经讨论,大家认为乙同学的猜想不正确,原因是_____;
②丙同学又提出了新的猜想,认为溶液中除氯化钠外,还可能含有_____,请你和丙同学一起验证他的猜想:
实验步骤 | 实验现象 | 实验结论 |
取少量无色溶液于试管_____ | _____ | 丙同学猜想正确 |
【题目】下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ | 20 | 40 | 60 | 80 | |
溶解度/g | 氯化钠 | 36.0 | 36.6 | 37.3 | 38.4 |
硝酸钾 | 31.6 | 63.9 | 110.0 | 169.0 | |
(1)两种物质中,溶解度的变化受温度影响较小的是_____。
(2)20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为_____。
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是_____。
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是_____。