题目内容
【题目】甲、乙、丙三种物质的溶解度曲线如图所示,回答下列问题:
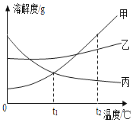
(1)三种物质中_____的溶解度随温度变化趋势与气体溶解度的变化相似(填“甲”或“乙”或“丙”)
(2)将t2℃时甲,乙两物质饱和溶液分别蒸发等质量的水,析出固体的质量甲____乙(填“>”或“<”或“=”)
(3)当甲中混有少量乙时,可采用______的方法提纯甲
(4)将t2℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由小到大的顺序为_______。
【答案】丙 大于 降温结晶 (冷却热饱和溶液) 甲乙丙
【解析】
(1)三种物质中丙的溶解度随温度变化趋势与气体溶解度的变化相似,都是溶解度随温度的升高而减少;
(2)将t2℃时,甲、乙两物质饱和溶液分别蒸发等质量的水,析出固体的质量甲>乙,因为在该温度下甲的溶解度大于乙;
(3)当甲中混有少量乙时,可采用降温结晶(或冷却热饱和溶液)的方法提纯甲,因为甲的溶解度受温度的影响变化比乙大;
(4)将t2℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为:丙>乙>甲,因为降温后,溶剂的质量不变。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案【题目】下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ | 20 | 40 | 60 | 80 | |
溶解度/g | 氯化钠 | 36.0 | 36.6 | 37.3 | 38.4 |
硝酸钾 | 31.6 | 63.9 | 110.0 | 169.0 | |
(1)两种物质中,溶解度的变化受温度影响较小的是_____。
(2)20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为_____。
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是_____。
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是_____。
【题目】下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | |
(1)两种物质中,溶解度受温度影响变化较大的是______(填化学式)。
(2)60℃时,按图示操作:

A中溶质是_______(填“饱和”或“不饱和”)溶液,C中溶液的总质量是________g。
(3)50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液________(填“大于”“等于”或“小于”) KNO3溶液。
(4)由表中数据可知,若KNO3和NaCl在T℃时具有相同的溶解度Xg,则X最小的取值范围是____(用数学表达式表示,下同),T最小的取值范围是______