题目内容
【题目】取一定量的氧化铁和氧化铜的混合物,向其中加入100g 9.8%的稀硫酸恰好完全反应。则原混合物中氧元素的质量是( )
A. 0.8g B. 1.6g C. 3.2g D. 6.4g
【答案】B
【解析】
氧化铁和氧化铜与稀硫酸反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;CuO+H2SO4═CuSO4+H2O;由于氧化铜和氧化铁的混合物与100克、9.8%的稀硫酸恰好完全反应,分析化学方程式可知氧化物中氧元素全部转变为水中的氧元素,计算出水的质量进而计算出所含氧元素的质量即可;
设生成水的质量是x:由方程式可以看出硫酸与生成水的关系为
H2SO4 ~H2O
98 18
100g×9.8% x![]() =
=![]()
x=1.8g
所以水中氧元素的质量为:1.8g×![]() ×100%=1.6g。故选B。
×100%=1.6g。故选B。

 寒假学与练系列答案
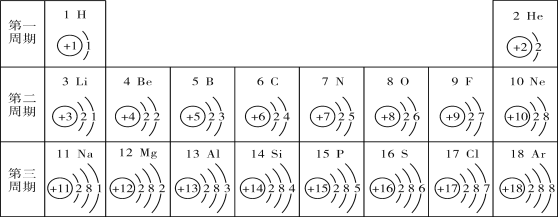
寒假学与练系列答案【题目】元素周期表是学习化学的重要工具,如表是元素周期表的一部分。请回答下列问题:
1 H | 2 He | ||||||
3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne |
11 Na | 12 Mg | 13 Al | 14 Si | 15 P | 16 S | 17 Cl | 18 Ar |
(1)元素周期表中不同种元素最本质的区别是_____(填序号)。
A.相对原子质量不同 B.质子数不同 C.中子数不同 D.元素符号不同
(2)镁元素的原子结构示意图为 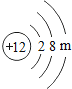 ,则m=_____,该原子在化学反应中易_____(填“得到”或“失去”)电子。说明元素的化学性质与原子的_____关系密切。
,则m=_____,该原子在化学反应中易_____(填“得到”或“失去”)电子。说明元素的化学性质与原子的_____关系密切。
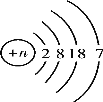
(3)元素周期表中每一个横行叫做一个周期。以第二周期为例,根据下图该周期中各元素的原子结构示意图,分析同一周期元素之间的排列有一定的规律,下面表述正确的是_____(填序号)。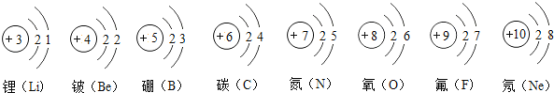
A.从左到右,各元素原子的电子层数相同
B.从左到右,各元素的原子序数依次递增
C.从左到右,各元素原子的最外层电子数相同
(4)由1号和8号元素组成的化合物(分子中原子个数比为2:1)与6号元素的单质,在高温下发生置换反应,生成一种最轻的气体和一种由双原子分子构成的化合物,该反应的化学方程式是_____。