题目内容
【题目】通过海水提取的粗盐中含有 MgCl2、CaCl2、MgSO4.以及泥沙等杂质.以下是一种 制备精盐的实验方案(用于沉淀的试剂均过量).
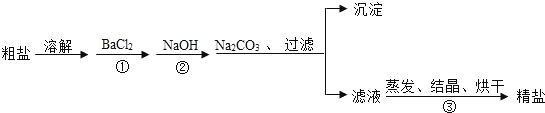
请回答下列问题:
(1)写出②中反应的化学方程式___________________________.
(2)加入 BaCl2、NaOH、Na2CO3 的顺序还可以改变吗?若能改变则写出改变的顺序,若不能改变,请说明理由_______________________________________.
(3)该实验方案还需完善,请写出具体的操作步骤___________________________________________.
【答案】2NaOH+MgCl2=Mg(OH)2↓+2NaCl BaCl2、Na2CO3、NaOH 向滤液中加入适量的稀盐酸
【解析】
(1)②中的反应是氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,化学方程式为:2NaOH+MgCl2=Mg(OH)2↓+2NaCl;
(2)氯化钡与硫酸镁反应生成硫酸钡和氯化镁,氯化钡的作用是除去硫酸镁;氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,氢氧化钠的作用是除去氯化镁;碳酸钠与氯化钡、氯化钙反应分别生成碳酸钡、碳酸钙和氯化钠,碳酸钠的作用是除去过量的氯化钡和氯化钙,碳酸钠必须放在氯化钡之后,与氢氧化钠的顺序部分先后,所以改变的顺序是:BaCl2、Na2CO3、NaOH;
(3)过滤后滤液的主要成分有:NaCl、NaOH、Na2CO3;要得到纯净的氯化钠,此实验方案尚需完善,具体步骤是:向滤液中加入适量的稀盐酸,以除去氢氧化钠和碳酸钠。
。

 阅读快车系列答案
阅读快车系列答案【题目】下表是三种物质在不同温度时的溶解度,根据表中信息回答问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
氢氧化钙 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(1)60℃时,氯化钠的溶解度_______硝酸钾的溶解度(填“>”“=”或“<”)。
(2)20℃时,氯化钠饱和溶液中溶质的质量分数为_______(结果保留至0.1%)。
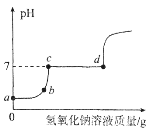
(3)如图所示,观察到U型管中a的液面低于b的液面,澄清石灰水_____________,则在小试管中加入的物质是_____(填字母)。
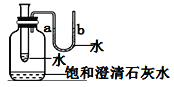
A.浓硫酸 B.氢氧化钠 C.硝酸铵
(4)混有少量氯化钠的硝酸钾固体,加水配成80℃的硝酸钾饱和溶液,再冷却至20℃,析出晶体并得到溶液。下列有关说法中正确的是_______(填字母)。
A.析出的晶体中不一定含有硝酸钾
B.所得溶液一定是硝酸钾饱和溶液
C.上述方法可以将两种物质完全分离
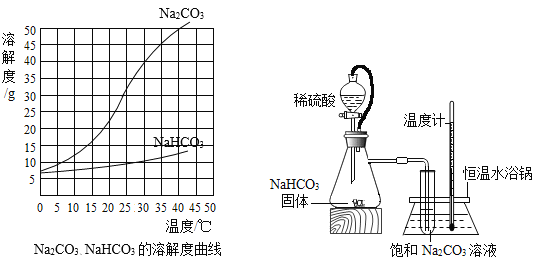
【题目】由于溶解度不同(如图所示),饱和碳酸钠溶液中通入CO 2会析出碳酸氢钠晶体而使溶液变浑浊。某化学课外小组同学发现不同条件下出现浑浊的时间不同。
(提出问题)影响碳酸氢钠晶体产生速率的因素有哪些?
(猜想与假设)碳酸氢钠晶体产生速率的影响因素有温度、试管内径、CO2流速、饱和碳酸钠溶液的体积。
(进行实验)实验装置如图所示。每次实验时均在试管里加入1mL饱和碳酸钠溶液并在试管后放置一张写有黑色字迹的白纸,从垂直于试管的方向观察白纸上字迹的清晰程度,记录时间,用于判断碳酸氢钠晶体的产生速率。部分实验记录如下表所示:
序号 | 温度(℃) | 试管内经(mm) | CO2流速 (个气泡/s) | 产生不同现象的时间(s) | ||
字迹变浅 | 字迹模糊 | 字迹消失 | ||||
① | 25 | 10 | 5~8 | 517" | 719" | 817" |
② | 32 | 10 | 5~8 | 350" | 409" | 428" |
③ | 40 | 10 | 5~8 | 348" | 406" | 418" |
④ | 25 | 14 | 5~8 | 636" | 738" | 828" |
⑤ | 25 | 25 | 5~8 | X | 943" | 1022" |
⑥ | 25 | 10 | 10~13 | 502" | 640" | 758" |
⑦ | 25 | 10 | 2~5 | 540" | 1045" | 1236" |
(解释与结论)
(1)由上述溶解度曲线图可知溶解度受温度影响相对更大的物质是_________________。
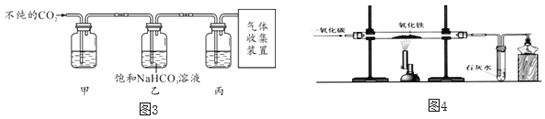
(2)锥形瓶中是利用碳酸氢钠与稀硫酸反应来制取二氧化碳。除生成二氧化碳外,还有水和硫酸钠生成,该反应的化学方程式为_____________________。
(3) 同学们若要研究饱和碳酸钠溶液的体积对碳酸氢钠晶体产生速率是否有影响,需要控制的变量有__________________。
(4)由实验①②③,可得出的结论是____________________。
(5)实验①④⑤研究的影响因素是___________________。
(6)通过对数据的观察和分析,小倩认为“二氧化碳流速越快,碳酸氢钠晶体产生速率越快”,得到该结论的依据是______________(填实验序号)。
(反思与评价)
(7)表中X的取值范围应该是_______________。
(8)该实验采用硫酸而不是盐酸来制备二氧化碳的原因是__________________。
(9)如图中使用橡皮管连接分液漏斗与锥形瓶的目的是__________________。
(10)如何除去碳酸钠中混有的少量碳酸氢钠?___________________。