题目内容
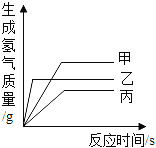
【题目】为了探究金属与酸反应的规律,某实验小组进行了如下实验,取等质量的铁片、镁片、锌片,分别与等体积、等浓度的稀盐酸反应,用温度传感器测得反应温度变化曲线如下图所示。
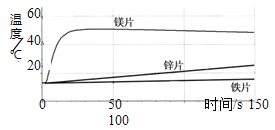
(1)请分析反应中温度升高的原因:_________________ ;
(2)根据曲线总结出金属活动性的相关规律:__________。
【答案】 金属与酸反应放出热量 相同条件下,金属越活泼,与酸反应放出的热量越多(必须指明条件相同
【解析】(1)根据金属与酸反应的规律可知:金属与酸反应过程中放出热量,使温度升高;(2) 根据温度传感器测得反应温度变化曲线可知,等质量的铁片、镁片、锌片,分别与等体积、等浓度的稀盐酸反应,放出热量的关系是:铁>镁>锌,由此可推知金属活动性的相关规律:相同条件下,金属越活泼,与酸反应放出的热量越多。

练习册系列答案
相关题目