题目内容
【题目】科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰(MnO2)粉末,然后加入等量的不同浓度的过氧化氢溶液,观察气泡产生的速度,记录如表:
实验次数 | 1 | 2 | 3 | 4 |
H2O2溶液的浓度 | 1% | 5% | 10% | 15% |
MnO2质量 | 0.2克 | 0.2克 | 0.2克 | 0.2克 |
气泡产生的速度 | + | ++ | +++ | ++++ |
(1)该实验研究的问题是:过氧化氢分解的速度与_____的关系.
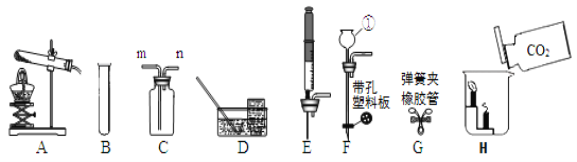
(2)为了检验产生的气体是否为氧气,请你写出检验的方法:____________________.
(3)过氧化氢和二氧化锰制氧气的基本反应类型是_______反应.如果要说二氧化猛在该反应中起到催化作用,还需要通过实验验证二氧化锰在反应前后________不变.
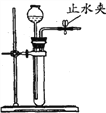
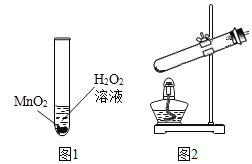
(4)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验征加热双氧水也可以产生氧气,同学们选择如图2装置(气密性良好)进行实验.实 验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是______________________.
【答案】 过氧化氢溶液的浓度 将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气 分解 质量和化学性质 氧气中混有较多的水蒸气
【解析】(1)由“四支试管中分别加入0.2克二氧化锰(MnO2)粉末,然后加入等量的不同浓度的过氧化氢溶液”可知该实验是探究过氧化氢分解的速度与浓度的关系;(2)氧气能使带火星的小木条复燃,故检验氧气的方法是将带火星的木条伸入试管中,如果木条复燃,则证明该气体为氧气;(3)过氧化氢在二氧化锰的催化作用下生成水和氧气,该反应属于分解反应;催化剂具有“一变二不变”的特点,即能改变物质的反应速率,但物质的质量和化学性质不变,故要说二氧化猛在该反应中起到催化作用,还需要通过实验验证二氧化锰在反应前后的质量和化学性质不变;(4)过氧化氢溶液中含有大量的水,加热后会产生大量的水蒸气,故伸入带火星的小木条不会复燃。