题目内容
【题目】人类历史发展的不同阶段曾以不同金属材料的使用作为标志。

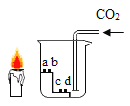
(1)金、银在自然界有单质形式存在,说明它们的化学性质都___________。
(2)在生产生活实践中人类逐渐掌握多种金属的技术。
①比较两种铁矿石磁铁矿(主要成分Fe3O4) 和菱铁矿(主要成分FeCO3), 从化学的角度分析“磁铁矿作炼铁原料更具优势”,其原因是___________。
②近代工业上采用电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质,该反应的化学方程式为____________。
(3)钛和钛合金是21世纪的重要的金属材料,钛合金制品放在海水中数年取出后仍光亮如新,是因为其____ (填序号) 非常好。
A 可塑性.
B 机械性能
C 抗腐蚀性能
(4)铁在潮湿的空气中反应生成疏松的铁锈,铁锈的主要成分是__________(填化学式)。
(5)利用“活泼金属”可以制得H2,H2可用作汽车能源,若推广应用于汽车产业,则需要综合考虑的因素有________(填序号)。
a 金属原料的成本
b 生产过程中的能源消耗和污染
c 金属的回收利用
【答案】不活泼 四氧化三铁中铁元素含量高于碳酸亚铁 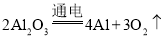 C Fe2O3 abc
C Fe2O3 abc
【解析】
电解熔融氧化铝生成铝和氧气,以单质形式存在的金属说明化学性质不活泼。
(1)以单质形式存在的金属说明化学性质不活泼,金、银在自然界有单质形式存在,说明它们的化学性质都不活泼。
(2)①要冶炼金属,金属元素含量高,产量也比较高,故原因是四氧化三铁中铁元素含量高于碳酸亚铁。
②电解熔融氧化铝(Al2O3)的方法冶炼铝,Al2O3分解后得到两种单质为铝和氧气,反应的化学方程式为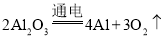 。
。
(3)钛合金制品放在海水中数年取出后仍光亮如新,说明抗腐蚀性能力强,故选C。
(4)铁锈是铁和氧气和水生成的,主要成分为氧化铁,化学式为Fe2O3。
(5)推广应用于汽车产业,则需要综合考虑的因素有成本、能源、回收问题,故选abc。

 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
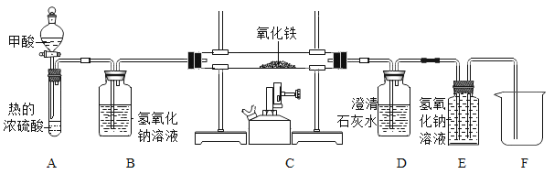
学习实践园地系列答案【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案。
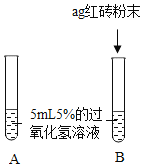
[提出问题]红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
[实验探究]
实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是_ ②___ |
II.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的__在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
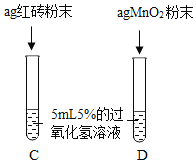
Ⅲ. | 两试管中均产生气泡且 __ | 红砖粉末的催化效果没有二氧化锰粉末好 |
[拓展应用]
己知CuSO4也可作为过氧化氢分解的催化剂。向101g 一定溶质质量分数的过氧化氢溶液中加入2gCuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气__g。
【题目】某矿石主要成分是 MgO,含少量的 Fe2O3、CuO 和 SiO2杂质。用该矿石制备Mg(OH)2的工艺流程简图如图:
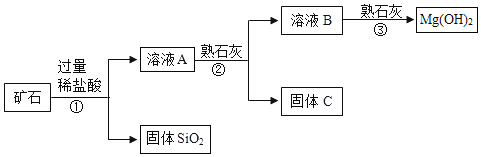
已知氢氧化铜、氢氧化铁和氢氧化镁均是沉淀,请回答下列问题:
(1)步骤①和步骤②均用到的操作是__________,需要的玻璃仪器有烧杯、漏斗和_____________。
(2)溶液 A 中所含的阳离子有 Fe3+、Cu2+、Mg2+和 __________(填离子符号)。
(3)已知部分金属阳离子以氢氧化物形成沉淀时溶液的 pH 见下表:
对应离子 | Fe3+ | Cu2+ | Mg2+ |
开始沉淀时的 pH | 1.9 | 4.2 | 9.1 |
完全沉淀时的 pH | 3.2 | 6.7 | 11.1 |
步骤②加入熟石灰,调节溶液的 pH 范围为_______________;固体 C 中所含固体成分的化学式为______________;该步骤②中所涉及的中和反应的化学方程式是______________。
(4)步骤③制取 Mg(OH)2的化学方程式为______________。