题目内容
【题目】课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案。
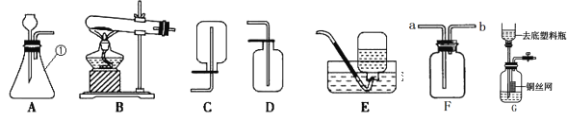
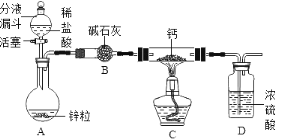
[提出问题]红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
[实验探究]
实验步骤 | 实验现象 | 实验结论及解释 |
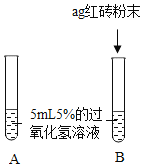
Ⅰ. | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是_ ②___ |
II.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的__在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
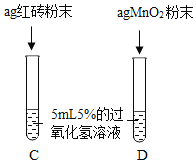
Ⅲ. | 两试管中均产生气泡且 __ | 红砖粉末的催化效果没有二氧化锰粉末好 |
[拓展应用]
己知CuSO4也可作为过氧化氢分解的催化剂。向101g 一定溶质质量分数的过氧化氢溶液中加入2gCuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气__g。
【答案】O2 红砖粉末能改变过氧化氢分解速率 质量和化学性质 D 试管速率比C快 3
【解析】
Ⅰ、根据“B中产生大量能使带火星木条复燃的气体”可知,说明生成的气体是氧气;根据实验A、B的现象可知,红砖粉末能改变过氧化氢分解速率;
Ⅱ、红砖粉末能作催化剂,说明反应前后的质量化学性质不变;
Ⅲ、红砖粉末的催化效果没有二氧化锰粉末好,则D试管速率比C快;
[拓展应用]
CuSO4粉末在化学反应中用作催化剂,在化学反应前后质量不变,充分反应后得到溶质质量分数为2%的溶液,溶质的质量=2g;则溶液的质量=2g÷2%=100g,溶剂水的质量=100g-2g=98g,根据质量守恒定律可知:生成的氧气质量=101g-98g=3g。

练习册系列答案
相关题目