题目内容
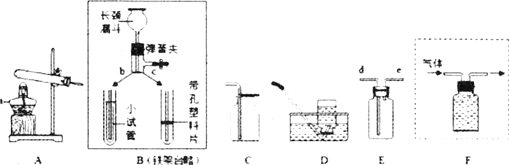
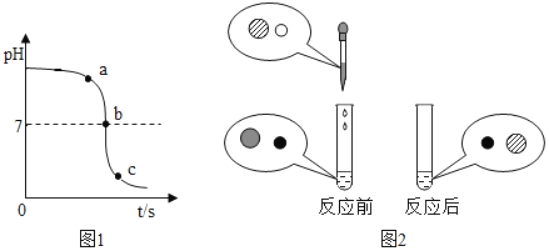
【题目】为探究盐酸的化学性质,某同学做了如图实验:

(1)试管A中的现象是______,B中反应的化学方程式为______。
(2)反应结束后,将A、B中的物质倒入同一个洁净的烧杯中,观察到烧杯中有气泡产生,反应结束后烧杯底有固体剩余。该同学们继续对反应后烧杯内的物质进行探究,他将烧杯内的物质过滤,得到滤液和滤渣。
(分析)滤液中一定含有的溶质是______。
(提出问题)滤渣的成分是什么?
(做出猜想)滤渣的成分是①______;②______。
(进行实验)该同学取少量滤渣于试管中,加入______。通过观察现象得出结论。
【答案】溶液由无色变为浅绿色,有气泡产生 CuO+2HCl=CuCl2+H2O 氯化亚铁 铜 铁 稀盐酸
【解析】
(1)A中稀盐酸和铁片发生反应生成氯化亚铁和氢气,可观察到的现象为溶液由无色变为浅绿色,有气泡产生,试管B中稀盐酸和氧化铜反应生成氯化铜和水,反应的化学方程为CuO+2HCl═CuCl2+H2O;
(2)反应结束后,将A、B中的物质倒入同一个洁净的烧杯中,观察到烧杯中有气泡产生,反应结束后烧杯底有固体剩余。该同学们继续对反应后烧杯内的物质进行探究,他将烧内的物质过滤,得到滤液和滤渣,可知铁和氯化铜反应生成氯化亚铁和铜单质;
则分析滤液中一定含有的溶质是氯化亚铁。
滤渣的成分是可能是铁,也可能是铜;
[进行实验]该同学取少量滤渣于试管中,加入稀盐酸。通过观察现象得到结论。
故填:(1)溶液由无色变为浅绿色,有气泡产生;CuO+2HCl═CuCl2+H2O;
(2)氯化亚铁;铜;铁;稀盐酸。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目