题目内容
【题目】某校化学小组在利用盐酸和氢氧化钾溶溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图象如图1所示
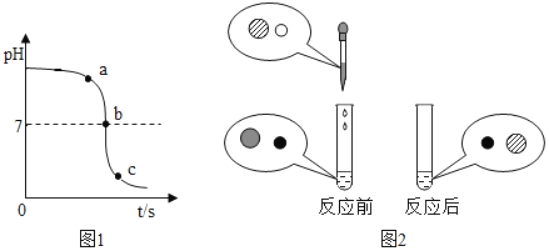
(1)该实验是将_____逐滴滴入到盛有_____溶液的烧杯中。
(2)图中a点所示溶液中,含有的溶质是_____ (写溶质的化学式)。
(3)图中a点到b点反应过程中滴入的酚酞由_____色变_____色。
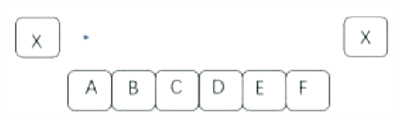
(4))反应前后溶液中存在的离子种类如图2所示(其中“![]() ”表示不同离子)
”表示不同离子)![]() 表示的离子为_____(写离子符号,下同)
表示的离子为_____(写离子符号,下同)![]() 表示的离子为_____。
表示的离子为_____。
(5)从微观角度看,该反应有效相互作用的微粒是_____(写微粒符号)
【答案】盐酸; 氢氧化钠; NaCl、NaOH; 红; 无; H+; Na+; H+与OH﹣
【解析】
(1)由图1中原溶液的pH大于7可知,该变化对应的实验操作是将盐酸滴加到氢氧化钠中;故填:盐酸;氢氧化钠;
(2)图中a点所示溶液的pH>7,即溶液显碱性,溶液中的溶质是氯化钠和氢氧化钠;故填:NaCl、NaOH;
(3)a点所示溶液的pH>7,显碱性,能使无色酚酞试液变红色,b点所示溶液的pH=7,呈中性,不能使无色酚酞试液变色;故填:红;无;
(4)氢氧化钠与稀盐酸反应生成氯化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子,由反应前后溶液中存在的离子种类图,此反应的实质是![]() 和
和![]() 结合生成水分子,向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,试管中的溶液是氢氧化钠溶液,则
结合生成水分子,向氢氧化钠溶液中滴加稀盐酸至恰好完全反应,试管中的溶液是氢氧化钠溶液,则![]() 表示氢氧根离子,胶头滴管中的溶液是稀盐酸,
表示氢氧根离子,胶头滴管中的溶液是稀盐酸,![]() 是钠离子,
是钠离子,![]() 表示的离子为氢离子;故填:H+;Na+;
表示的离子为氢离子;故填:H+;Na+;
(5)氢氧化钠与稀盐酸反应生成氯化钠和水,中和反应的实质是氢离子和氢氧根离子结合生成水分子。故填:H+与OH﹣。

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目