题目内容
【题目】98g质量分数为10%的硫酸溶液跟一定质量的氢氧化钠溶液恰好完全反应,在得到的溶液中,硫酸钠的质量分数为10%,试求:
(1)硫酸钠溶液的质量_____;
(2)氢氧化钠溶液中溶质的质量分数_____。
【答案】142克 18.2%
【解析】
根据氢氧化钠与硫酸反应的化学方程式和参与反应的H2SO4的质量,即可计算出反应生成Na2SO4的质量(即溶质质量)和参与反应的氢氧化钠的质量。然后根据质量守恒定律(在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和),反应前硫酸溶液的质量+参与反应的氢氧化钠溶液的质量=生成硫酸钠溶液的质量,然后根据溶质质量分数公式计算即可。
解:(1)设反应生成Na2SO4的质量为x,参与反应的氢氧化钠的质量为y,98克质量分数为10%的稀硫酸中H2SO4的质量为98g×10%=9.8g,
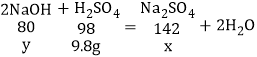
![]() x=8g,
x=8g,
![]() y=14.2g,
y=14.2g,
生成硫酸钠溶液的质量=![]() =142g;
=142g;
(2)氢氧化钠溶液中溶质的质量分数为![]() ≈18.2%;
≈18.2%;
答:(1)生成硫酸钠溶液的质量为142克;
(2)氢氧化钠溶液中溶质的质量分数为18.2%。

练习册系列答案
相关题目
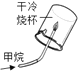
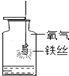
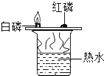
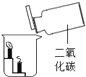
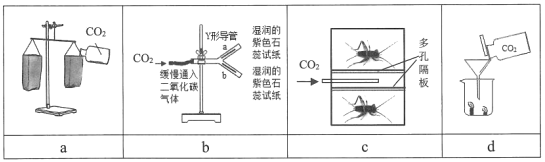
【题目】根据下图所示实验分析得出的结论中,不正确的是( )
|
|
|
|
A.甲烷燃烧生成二氧化碳和水 | B.铁能在氧气中燃烧 | C.白磷的着火点比红磷的低 | D.二氧化碳的密度比空气大,不燃烧也不支持燃烧 |
A. A B. B C. C D. D