题目内容
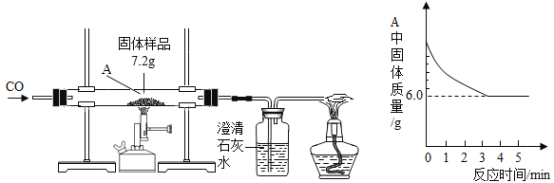
【题目】学习完酸碱盐的知识后,某化学兴趣小组同学在实验室做如图所示实验,小明取2mLNa2CO3溶液于试管中,滴入少量稀盐酸,无明显现象(如图1);小英取2mL稀盐酸于试管中,滴入少量Na2CO3溶液,却观察到立即有气泡产生(如图2)。两人实验所用的Na2CO3溶液、稀盐酸均相同,却观察到不同的实验现象,为此,他们进行了如下探究。
(提出问题)小明实验后溶液中的溶质是什么?
(作出猜想)①NaCl;②NaCl、 NaHCO3;③ NaCl Na2CO3;④NaCl、Na2CO3 NaHCO3
(查阅资料)
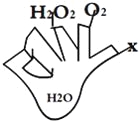
a.HCl和Na2CO3反应是分步进行的,即:
![]()
![]() (后)。
(后)。
说明上述猜想__________一定不成立(填序号);
b. NaHCO3溶液与足量澄清石灰水混合会变浑浊;
c.Ca(HCO3)2溶于水。
(实验探究)
实验操作 | 实验现象 | 结论 |
取适量小明实验后的溶液于试管中滴入澄清石灰水 | 溶液变浑浊 | 猜想④成立 |
(交流反思)(1)请分析上述实验探究结论是否正确,并说明原因________________________________。
(2)请设计一个实验来验证剩余猜想。
实验操作 | 实验现象 | 结论 |
猜想______成立 |
(归纳总结)小明实验与小英实验现象不同的主要原因为________________________________。
【答案】①③ 不正确,因为溶液中的碳酸氢钠与澄清石灰水混合也会出现浑浊 取适量小明实验后的溶液于试管中,继续滴入稀盐酸一开始无明显现象,一段时间后观察到有气泡产生(或开始就有气泡产生)④(或②,与上一空对应) 稀盐酸的质量不同
【解析】
[作出猜想]当加入少量稀盐酸时,碳酸钠与稀盐酸反应生成氯化钠、碳酸氢钠,因此小明实验后溶液中一定含有反应生成的氯化钠、碳酸氢钠,可能含有反应剩余的碳酸钠,因此猜想①、③错误;
[交流反思](1)根据资料可知, NaHCO3溶液与足量澄清石灰水混合会变浑浊,因此根据溶液变浑浊的现象不可直接确定溶液中含有碳酸钠;
(2)结合查阅资料的内容,当滴入少量稀盐酸时,碳酸钠先与稀盐酸反应生成氯化钠、碳酸氢钠,无明显变化,继续滴入稀盐酸,当碳酸钠消耗完后,碳酸氢钠与稀盐酸反应生成二氧化碳,产生气泡;所以实验方案:取适量小明实验后的溶液,滴加少量盐酸;现象:立即产生气泡;结论:猜想②成立;
[归纳总结]根据前面的分析,可知二者实验现象不同的主要原因是与碳酸钠接触的稀盐酸的质量不同。

 小学课时特训系列答案
小学课时特训系列答案【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是( )
A | B | C | D | |
实验装置 |
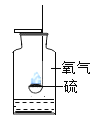
硫在氧气中燃烧 |
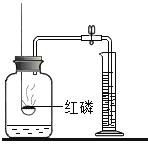
测定空气中氧气含量 |
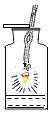
铁丝在氧气中燃烧 |
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热 | 量简中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 集气瓶中的水:先将集气瓶内的空气排净,后便于观察H2何时收集满 |
A.AB.BC.CD.D
【题目】某化学活动小组在一次探究复分解反应的实验活动中,选取了下表中四种化合物的溶液相互反应,它们之间能发生反应但无明显现象的是___________________________(填序号)。
A | B | C | D |
氢氧化钠溶液 | 稀盐酸 | 碳酸钠溶液 | 氯化钡溶液 |
实验结束后,小组同学将废液倒入废液缸中。将废液缸内的物质过滤后,对滤液成分进行了进一步的探究。小组同学经认真分析,推出废液中一定含有Na+、Cl -。欣欣同学按图示取少量废液于试管中滴入无色酚酞试液,发现溶液变红。
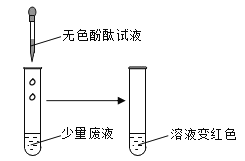
[提出问题]废液缸中的废液中还含有哪些离子?
[猜想与假设]
猜想1:废液中还含有OH-、CO32- ;
猜想2:废液中还含有OH-、Ba2+;
猜想3:废液中还含有CO32- ;
猜想4:废液中还含有 ______________(填离子符号,下同)
[实验探究]
实验操作 | 实验现象 | 实验结论 | |
甲同学 | 取少量废液于试管中,向其中滴加足量稀盐酸 | 观察到有气泡冒出 | 废液中一定含有 _________________________ 。 |
乙同学 | 另取少量废液于试管中,向其中滴加足量 ___________________ ,再滴加无色酚酞试液 | 可观察到溶液中产生白色沉淀 _____________________ 。 | 猜想1成立 |
[讨论交流]甲同学的实验中观察到产生气泡时所发生反应的化学方程式为 ______________________ 。
[评价与反思]在实验探究环节中,加入的试剂均足量,请写出原因 _____________________