题目内容
【题目】某K2CO3样品中含有Na2CO3、NaCl、Ca( NO3)2三种杂质中的一种或两种。现取13. 8 g样品加入足量水,样品全部溶解,再加入过量的CaCl2溶液,得到9g沉淀。对样品所含杂质的判断正确的是
A.肯定只有Na2CO3
B.肯定只有NaCl
C.肯定有NaCl,可能还含有Na2CO3
D.肯定没有Ca(NO3)2
【答案】CD
【解析】
样品加入足量水,全部溶解,由于硝酸钙能与碳酸钾反应产生沉淀,故样品中一定没有硝酸钙,根据题干提供的数据,假设样品全部是碳酸钾或碳酸钠,求出生成沉淀的质量,再判断物质的成分。
设13.8g碳酸钾与氯化钙反应生成碳酸钙的质量为x
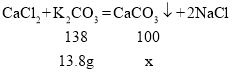
![]()
x=10 g,将产生10 g碳酸钙沉淀。
设13.8g碳酸钠与氯化钙反应产生碳酸钙的质量为y
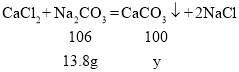
![]()
y≈13 g,将产生约13g的沉淀。
若杂质只含有碳酸钠,则得到沉淀的质量应该大于10 g小于13 g,而实际只得到9 g,说明样品中不可能只含有碳酸钠杂质;样品中的杂质可能只有氯化钠,或氯化钠和碳酸钠。
A.由分析可知,样品中的杂质为氯化钠,或氯化钠和碳酸钠,选项错误;
B.样品中可能同时含有氯化钠和碳酸钠杂质,选项错误;
C.由分析可知,样品中肯定含有氯化钠,可能含有碳酸钠选项正确;
D.样品加入足量水,全部溶解,由于硝酸钙能与碳酸钾反应产生沉淀,故样品中一定没有硝酸钙,选项正确;
故选:CD。

 阅读快车系列答案
阅读快车系列答案【题目】元素周期表是学习化学的重要工具。下表中列出了部分元素的原子序数,回答下列问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
第一周期 | 1 | 2 | ||||||
第二周期 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
第三周期 | 11 | 12 | Al | 14 | 15 | 16 | 17 | Ar |
(1)表中铝元素原子的核内质子数为________。
(2)18号元素的原子结构示意图为________。
(3)9号和12号元素形成的化合物的化学式为________。
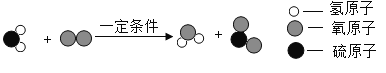
(4)下图是某化学反应的微观示意图,该反应的化学方程式为________。
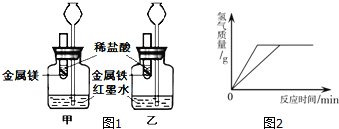
【题目】实验室中有一瓶放置时间较长的石灰水,在瓶口有很厚的白色固体,对白色固体同学们作了如下的假设:

①是CaCO3。②是Ca(OH)2。你认为第③种假设可以是________________。请你完成下列的实验报告:
实验步骤 | 实验现象 | 结论 |
1.将白色固体加入_____试剂中。 | 试剂变红色。 | ________ |
2.另取少量白色固体放入试管A中,加入足量盐酸后迅速连接试管(如图所示)。 | B中观察到澄清石灰水变浑浊。 | ________ |
通过上述实验可以证明这一白色固体是________,试管A中发生反应的化学方程式为________。 |
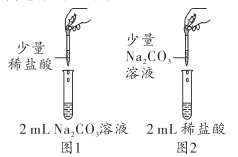
【题目】学习完酸碱盐的知识后,某化学兴趣小组同学在实验室做如图所示实验,小明取2mLNa2CO3溶液于试管中,滴入少量稀盐酸,无明显现象(如图1);小英取2mL稀盐酸于试管中,滴入少量Na2CO3溶液,却观察到立即有气泡产生(如图2)。两人实验所用的Na2CO3溶液、稀盐酸均相同,却观察到不同的实验现象,为此,他们进行了如下探究。
(提出问题)小明实验后溶液中的溶质是什么?
(作出猜想)①NaCl;②NaCl、 NaHCO3;③ NaCl Na2CO3;④NaCl、Na2CO3 NaHCO3
(查阅资料)
a.HCl和Na2CO3反应是分步进行的,即:
![]()
![]() (后)。
(后)。
说明上述猜想__________一定不成立(填序号);
b. NaHCO3溶液与足量澄清石灰水混合会变浑浊;
c.Ca(HCO3)2溶于水。
(实验探究)
实验操作 | 实验现象 | 结论 |
取适量小明实验后的溶液于试管中滴入澄清石灰水 | 溶液变浑浊 | 猜想④成立 |
(交流反思)(1)请分析上述实验探究结论是否正确,并说明原因________________________________。
(2)请设计一个实验来验证剩余猜想。
实验操作 | 实验现象 | 结论 |
猜想______成立 |
(归纳总结)小明实验与小英实验现象不同的主要原因为________________________________。