题目内容
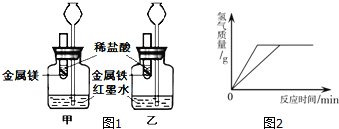
【题目】某化学小组的同学们对一份固体样品进行了探究。通过实验已确定该样品由氧化铁和铁粉混合而成。他们取了7.2g固体样品,用图1所示的装置继续实验,测定的部分数据如图2所示。
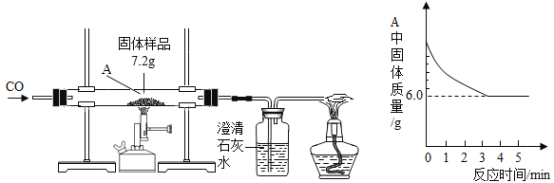
图1 图2
请计算:
(1)该样品中铁粉的质量分数。(计算结果精确到0.1%)
(2)该样品中铁元素与氧元素的质量比。
【答案】(1)44.4%
(2)5:1
【解析】
(1)【方法1】解:设氧化铁的质量为x。
3CO + Fe2O3 ![]() 2Fe + 3CO2 固体减重
2Fe + 3CO2 固体减重
160 112 48
x (7.2 g-6 g)
![]() =
=![]()
x=4g ┄┄┄┄(1分)
Fe%=![]() =44.4% ┄┄┄┄(1分)
=44.4% ┄┄┄┄(1分)
【方法2】
固体减重:7.2 g-6g==1.2g
即为氧化铁中氧元素的质量,则氧化铁的质量为 1.2g÷![]() =4g
=4g
Fe%=![]() =44.4%
=44.4%
(2)Fe元素总质量:(7.2 g-4 g)+4g×![]() =6g
=6g
O元素总质量:4g×![]() =1.2g
=1.2g
m(Fe):m(0)=6g:1.2g=5:1 ┄┄┄┄

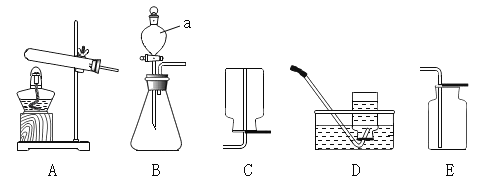
【题目】学习完酸碱盐的知识后,某化学兴趣小组同学在实验室做如图所示实验,小明取2mLNa2CO3溶液于试管中,滴入少量稀盐酸,无明显现象(如图1);小英取2mL稀盐酸于试管中,滴入少量Na2CO3溶液,却观察到立即有气泡产生(如图2)。两人实验所用的Na2CO3溶液、稀盐酸均相同,却观察到不同的实验现象,为此,他们进行了如下探究。
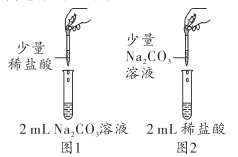
(提出问题)小明实验后溶液中的溶质是什么?
(作出猜想)①NaCl;②NaCl、 NaHCO3;③ NaCl Na2CO3;④NaCl、Na2CO3 NaHCO3
(查阅资料)
a.HCl和Na2CO3反应是分步进行的,即:
![]()
![]() (后)。
(后)。
说明上述猜想__________一定不成立(填序号);
b. NaHCO3溶液与足量澄清石灰水混合会变浑浊;
c.Ca(HCO3)2溶于水。
(实验探究)
实验操作 | 实验现象 | 结论 |
取适量小明实验后的溶液于试管中滴入澄清石灰水 | 溶液变浑浊 | 猜想④成立 |
(交流反思)(1)请分析上述实验探究结论是否正确,并说明原因________________________________。
(2)请设计一个实验来验证剩余猜想。
实验操作 | 实验现象 | 结论 |
猜想______成立 |
(归纳总结)小明实验与小英实验现象不同的主要原因为________________________________。
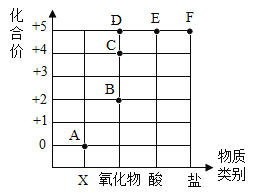
【题目】化学与生活息息相关。
自热米饭的营养成分表
营养素 | 每份含量 |
油脂 | 23.5g |
糖类 | 104.7g |
维生素 | 3.5g |
钠 | 814mg |
钙 | 130mg |
水 | 小于210g |
(1)自热米饭是一种快餐食品。请根据如图及表信息,回答下列问题:

①从“自热米饭的营养成分表”看,表中没有标出的人体必须的营养素是_________;
②图 1 包装材料是符合卫生标准的铝箔。铝被压制成铝箔,说明铝具有良好的_________性;
③该自热米饭是利用发热包中的生石灰与水反应放出热量来进行加热,生石灰与水反 应的化学方程式为__________。
(2)良好的家居环境带来美好的生活。
①房屋装修后,可在室内放一些活性炭来吸收装修材料释放出的甲 醛、苯等有毒气体,这是利用活性炭的___________性。
②如图,“火立熄”是一种新型的家用灭火用品。“火立熄”接 触到火焰 3-5 秒后炸开,释放的粉末覆盖在燃烧物上,同时放出 不可燃烧气体,使火焰熄灭。“火立熄”的灭火原理是____________。