题目内容
【题目】“元旦”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
(提出问题)锌与硫酸反应的快慢受哪些因素影响呢?
(猜想与假设)a.可能与硫酸的质量分数有关; b.可能与锌的形状有关。
(设计并实验)小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验编号 | 硫酸的质量分数 (均取20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式__________。
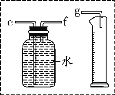
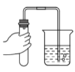
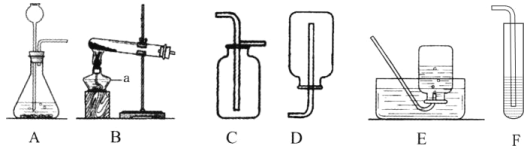
小兵用如图装置收集并测量氢气的体积,量筒的作用是_____,氢气应从_____(填e或f或g)管通入。
(收集证据)(3)比较不同浓度的硫酸对反应快慢的影响,选择的编号是_______。
(得出结论)(4)结论是_______。
(评价与反思)(5)下表是小兵第①组实验的详细数据。
时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
请描述锌与硫酸反应快慢的变化并解释原因______。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。_____。
【答案】Zn+H2SO4=ZnSO4 + H2↑ 接收水测量氢气体积,氢气应从f管通入 选择的编号是①③或②④ 其他条件相同时,稀硫酸浓度越大,反应越快 先加快,后减慢。反应放热,温度升高,速率增大,其后酸的浓度降低,速率减小 温度或锌的纯度等,在控制变量的条件下 温度;取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间
【解析】
(1)根据稀硫酸与锌反应产生硫酸锌和氢气进行分析;
(2)为测定所收集氢气的体积,则需要采用液体等量代换的方式,因此可以选用右图这样的装置,短进长出,让里面的水等量流到量筒内,通过量筒内液体的体积判断收集的气体的体积;
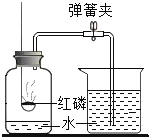
(3)根据二氧化碳会与水反应进行分析;
(4)对比四个实验,利用控制变量法选择合适的对比组;
(5)通过不同质量分数的硫酸与锌反应产生氢气的快慢得出结论;
(6)根据表格的数据总结产生的氢气与时间的关系并分析原因;
(7)反应物浓度、反应温度、反应物接触面积、有无催化剂等因素常影响化学反应速率,利用控制变量的思想设计一个因素对反应速率的影响。
(1)稀硫酸与锌反应产生硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
(2)因为氢气不易溶于水,可以通过压强的变化利用排水法把水压入量筒内,根据进入量筒中水的体积,判断生成氢气的体积,所以进气管是短管f;
(3)二氧化碳会与水反应,所以用该收集CO2,并测量生成的CO2气体的体积,其中在水面上放一层植物油目的是:防止二氧化碳与水反应;
(4)要比较不同质量分数的硫酸对反应快慢的影响,其中的锌的状态保持不变,选择不同质量分数的硫酸,看产生氢气的快慢,因此可以选择①③或②④;
(5)通过①③(都是锌粒,硫酸的质量分数不同),可以看出:硫酸的质量分数越大,反应速率越快;通过①②(锌粒和锌片与质量分数相同的硫酸反应)可以看出:锌与硫酸的接触面积越大,反应速率越快;
(6)从表格可以看出反应由慢到快然后逐渐减慢;因为随着反应的进行,反应放出热量,反应速度加快,但随着硫酸被消耗,硫酸溶质质量分数变小,反应速度又逐渐减慢;
(7)如设计温度对反应快慢的影响,具体的操作为:取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间。

 新黄冈兵法密卷系列答案
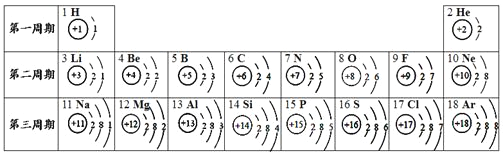
新黄冈兵法密卷系列答案【题目】元素周期表是化学学习的重要工具,依据下表回答问题:
|
|
(1)表中14号元素属于___(填元素名称,后同)元素,该元素的化学性质与____元素相似。
(2)通过上表的分析可知:元素所在的周期数=该元素原子核外的______。
(3)在化学反应中,铝原子失电子形成铝离子,写出铝离子符号______。