题目内容
【题目】如图是A、B、C三种固体物质的溶解度曲线,试看图后回答:
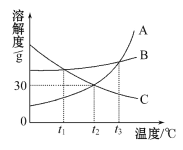
(1)在t3℃时,三种物质的溶解度的大小顺序是:______;
(2)在________时,B与C的溶解度相等;
(3)要从A、B、C的混合物中分离出A,最好用_______法;
(4)在温度介于t1℃和t2℃之间时,溶解相同质量的A、B、C,需要水的质量最小的是_____;
(5)t2℃时,将20 g A放入50 g水中充分溶解后,所得溶液质量是________g;
(6)我国北方有许多盐碱湖,湖水中溶有大量的氯化钠和纯碱(碳酸钠Na2CO3),那里的农民 “冬天捞碱,夏天晒盐”,其中“冬天捞碱”的道理是 __________。
【答案】A=B>C t2℃ 降温结晶 B 65g 碳酸钠的溶解度受温度影响大,冬天温度降低,其溶解度减小而从湖水中结晶析出(降温结晶)
【解析】
(1)根据三种物质的溶解度曲线可知,在t3℃时,A、B、C三种物质的溶解度从小到大的顺序是A=B>C;
(2)在t2℃时,B与C的溶解度曲线交于一点,二者的溶解度在该温度下相等;
(3)三种物质中AB的溶解度随温度降低而增大,C的溶解度随温度降低而减小,所以 要从含A、B、C的混合物中分离出C,最好采用冷却热饱和溶液或降温结晶的方法;
(4)在温度介于t1℃和t2℃之间时,A、B、C的溶解度关系为B>C>A,即在100g水中溶解的B最多,所以:溶解相同质量的A、B、C,需要水的质量最小的是B;
(5)t2℃时,A的溶解度是30g,即在100g水中最多溶解30gA,50g水最多溶解A的质量为15g,所得溶液质量=50g+15g=65g;
(6)因为Na2CO3的溶解度随温度升高而增大,而NaCl的溶解度受温度影响较小,因此冬天气温较低,析出的是Na2CO3晶体,而夏天气温高,当蒸发溶剂时,析出的主要是NaCl。