题目内容
【题目】食盐是一种重要的化工原料。粗盐中常含有少量的CaCl2、MgCl2、Na2SO4等杂质,将粗盐进行精制的流程如下图:
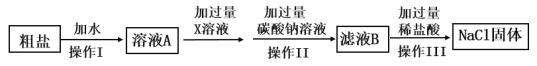
(1)过量X(纯净物)溶液中的溶质是_________________。
(2)加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠溶液,还有一个作用是_______(用化学方程式表示。)
(3)在操作III中玻璃棒的作用是什么___________?
【答案】氢氧化钠 HCl+NaOH═NaCl+H2O 搅拌,防止局部温度过高,造成液滴飞溅
【解析】
镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;完全反应后,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子。
(1)过量X(纯净物)溶液中的溶质是氢氧化钠。
(2)加入过量稀盐酸的目的可以除去滤液中过量的碳酸钠溶液,还有一个作用是除去过量的氢氧化钠,稀盐酸与氢氧化钠反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH═NaCl+H2O。
(3)操作Ⅲ是蒸发操作,玻璃棒的作用是搅拌,防止局部温度过高,造成液滴飞溅。

 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案【题目】在一次课外实验探究中,同学们将打磨过的镁条放到装有蒸馏水的试管中,发现镁条表面有极少量气泡(如图)。
(提出问题)产生的气体是什么?
(查阅资料)任意化学反应中,有元素化合价升高,必有元素化合价降低。
(猜想与假设)小红猜:O2:小明猜_____。
(实验1)
实验步骤 | 现象 | 结论 |
往镁与水反应的试管中滴 加2滴无色酚酞溶液 | 镁条附近溶液变红 | 生成了_____ |
请结合以上的探究内容和资料,写出镁与水的反应方程式:_____。
(实验2)同学们又做了镁条与盐溶液反应的实验,实验现象如表:
实验序号 | 实验1 | 实验2 |
与镁反应的试剂 | NaCl溶液 | H2O |
实验现象 | 有较多气泡产生 | 气泡极少 |
表中,用水进行实验的目的是_____,根据表中的实验现象,请设计一个实验方案证明是氯离子(C1﹣)而不是钠离子(Na+)能够加快镁与水的反应速率:_____。