题目内容
【题目】下列四个图象分别对应四种操作过程,其中正确的是( )
A. 双氧水分解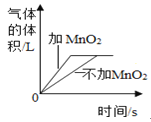
B. 向饱和氯化钠溶液中加水稀释
C. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应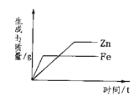
D. 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出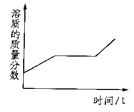
【答案】A
【解析】
A、实验室用过氧化氢制取氧气时,加入的催化剂二氧化锰能加快反应的速率,不会改变气体的质量,图像与事实相符,故A正确;
B、向饱和氯化钠溶液中加水稀释,氯化钠的质量不变,图像与事实不相符,故B错误;
C、常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应,锌比铁活泼,锌和稀硫酸反应时间短,最终铁和稀硫酸反应生成的氢气多,图像与事实不相符,故C错误;
D、硝酸钾不饱和溶液随着水分的蒸发,先形成饱和溶液,溶质的质量分数增大,当溶液达到饱和溶液以后,再蒸发,有晶体析出,质量分数保持不变,图像与事实不相符,故D错误。故选A。

【题目】化学兴趣小组为验证质量守恒定律,他们在老师指导下,做了镁条在空气中燃烧的实验。
(1)写出镁条与氧气反应的化学方程式:_____。
(2)小华发现燃烧所得固体的质量大于消耗的镁条质量,他据此认为该反应不遵循质量守恒定律。你_____(同意”或“不同意”)小华的观点,理由是_____。
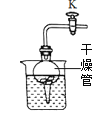
(3)小红按如图装置进行实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。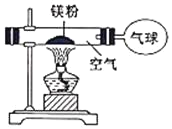
(提出问题)黄色固体是什么物质?
(查阅资料)①镁与氮气反应生成黄色的氮化镁(Mg3N2)固体;②氮化镁可与水剧烈反应产生氨气。
(做出猜想)黄色固体为氮化镁。
(实验探究)请你设计实验,验证猜想:
实验操作 | 实验现象 | 实验结论 |
取足量的黄色固体加入试管,然后滴入适量的_____,并将_____放在试管口 | _____ | 猜想正确 |
(反思与交流)
①通过上述探究活动,你对燃烧有什么新认识:_____。
②空气中氮气的含量远大于氧气的含量,而镁条在空气中燃烧生成的氧化镁却远多于氮化镁,这是因为_____。