题目内容
【题目】高纯MnCO3是制备电信器材高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
[查阅资料]
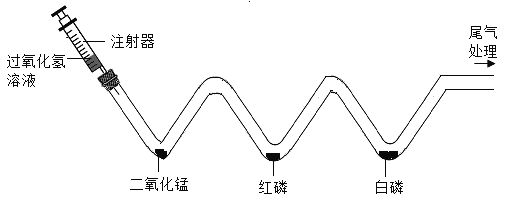
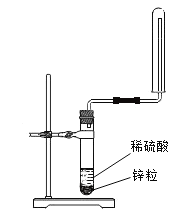
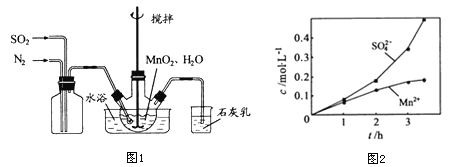
①向烧瓶中(见图1)通入过量混合气进行“浸锰”操作,主要反应原理为:![]() ;
; ![]()
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末。
③用Na2CO3溶液调节pH为3.5左右,过滤。
④调节滤液pH为6. 5~7.2,加入NH4HCO3,观察到有少量气体生成,有浅红色的沉淀生成,过滤、洗涤、干燥,得到高纯碳酸锰。
⑤H2SO3和O2在催化剂的催化作用下生成H2SO4。
[实验探究]
(1)①图1中应该先通入________一段时间后再通入___,原因是_____,石灰乳的作用是_____(用化学方程式表示)。
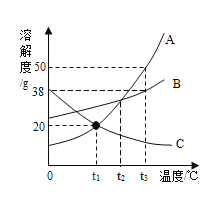
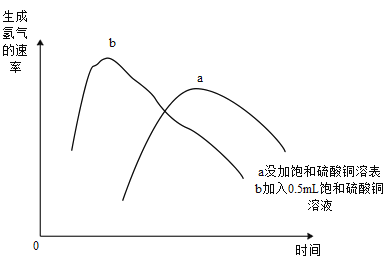
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图2所示,导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是_______,此时Mn2+的作用是_______。
③反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施是____(写出一 条即可)。
(2)加入的NH4HCO3与MnSO4溶液发生反应,请写出其化学方程式________。
【答案】N2 SO2 排尽装置中的空气防止干扰实验 ![]() Mn2+催化O2与 H2SO3反应生成了H2SO4 催化作用 控制温度或缓慢通入混合气体
Mn2+催化O2与 H2SO3反应生成了H2SO4 催化作用 控制温度或缓慢通入混合气体 ![]()
【解析】
(1)①图1中应该先通入氮气一段时间后,再通入二氧化硫气体,原因是:排尽装置中的空气,防止干扰实验,石灰乳(氢氧化钙)能与二氧化硫反应产生亚硫酸钙沉淀和水的化学方程式:![]() 。
。
②若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如图2所示,导致溶液中Mn2+、SO42-浓度变大的原因是:Mn2+能催化空气中的氧气与 H2SO3反应生成了H2SO4,此时Mn2+的作用是:催化作用;
③反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施是:控制温度或缓慢通入混合气体,使SO2尽可能转化完全;
(2)加入的NH4HCO3与MnSO4溶液发生反应产生硫酸铵、碳酸锰沉淀、二氧化碳气体和水的化学方程式:![]() 。
。

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】下列有关物质的检验、区分、分离、提纯所用的试剂或方法错误的是
选项 | 实验目的 | 所用试剂或方法 |
A | 检验 | NaOH溶液或 |
B | 除去生石灰中含有杂质石灰石 | 水或稀盐酸 |
C | 从 | 过滤或蒸发 |
D | 区分失去标签的浓硫酸和稀硫酸 | 水或小木条 |
A. A B. B C. C D. D
【题目】某校化学兴趣小组为测定黄铜中锌的质量分数,进行如下实验:
实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取黄铜样品加入烧杯中,使之与盐酸恰好完全反应 | ④特反应完全后,称重 |
实验图示 |
| |||
实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为150.0g | 黄铜样品的质量为20.0g | 烧杯和其中混合物的量为169.6g |
涉及反应的化学方程式:Zn+2HCl==ZnCl2+H2↑请完成下列问题:
(1)步骤③可观察到的现象是:_____。
(2)该实验中生成的氢气的质量是_____g。
(3)求该黄铜样品中锌的质量分数。