题目内容
【题目】元素周期表是学习和研究化学的重要工具。回答下列问题:
(1)元素周期表中不同元素间最本质的区别是______(填字母)。
A 质子数不同 B 中子数不同 C 相对原子质量不同
(2)元素周期表中氟元素的有关信息如下图所示,下列说法正确的是____(填字母)。
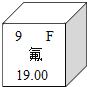
A 氟属于金属元素
B 氟的原子序数是9
C 氟的相对原子质量是19.00g
D 氟与氢组成的化合物的化学式为HF,其中F的化合价为-1价
【答案】A BD
【解析】
(1)由元素的概念可知,决定原子所属元素种类的是原子核内的质子数,即质子数相同的原子属于同一种元素,故填A。
(2)A 氟元素名称带有气字头,属于非金属元素,选项错误;
B 元素周期表中元素信息图中左上角的数字就是元素的原子序数,所以图中氟的原子序数是9,选项正确;
C 元素周期表中元素信息图中正下方的数字就是元素原子的相对原子质量,相对原子质量是一个比值,单位为“1”,常省略不写,所以氟的相对原子质量是19.00,选项错误;
D 氢元素的化合价为+1价,氟元素的化合价为-1价,根据化合物中各元素的化合价的代数和为零,所以氢元素与氟元素形成的化合物的化学式写为HF,选项正确,故填BD。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】兴趣小组想测定某铁合金中铁的含量,做了如下实验,称取14克样品,放入质量为50克的烧杯中,再往烧杯中加入100克足量的稀硫酸(杂质碳不与酸反应,也不溶于水),
并对烧杯进行了四次称量,记录数据如下:
反应时间 | T0 | T1 | T2 | T3 |
烧杯总质量(克) | 164 | 163.8 | 163.6 | 163.6 |
求(1)反应产生的氢气的质量是多少?
(2)该样品中铁的质量分数是多少?
(3)反应后所得溶液中溶质质量分数是多少?(要求写出计算过程,结果精确到0.1%)
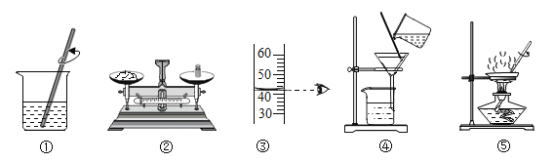
【题目】实验室部分装置如图所示,回答下列问题。
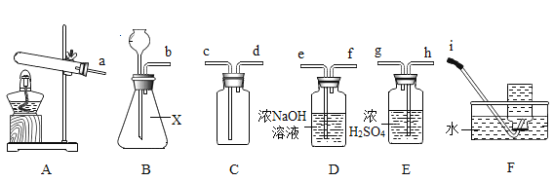
(1)实验室可用高锰酸钾在装置A中制氧气,其化学方程式为__。
(2)实验室用金属锌和稀盐酸反应制取H2,其化学方程式为____,为了得到纯净干燥的H2,请从中选择合适的装置,并按照顺序组装整套装置B→__→____ →C.用装置C收集H2时,气体从___管口通入装置C。
(3)实验室制取二氧化碳的化学方程式为____,制得的二氧化碳气体中含有氯化氢,可将 气体通入饱和碳酸氢钠溶液除去其中的氯化氢,其原理用方程式表示为____。欲收集较纯净的二氧化碳可采用的收集装置是___(填写装置序号)。
(4)某兴趣小组对KClO3分解分解制取氧气的反应催化剂进行研究,在相同的加热条件下,获得如下数据。
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mL O2所需时间/s |
实验1 | 5 | — | — | 176 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 68 |
实验4 | 5 | KCl | 0.5 | 135 |
①表中所列3种催化剂中催化效果最佳的是______。
②由实验1和实验4可知,KCl____(填“有”或“无”)催化作用。
③为准确直观比较分解速率的快慢,除测定收集一定体积的O2所需时间,还可以测定________。