题目内容
【题目】40℃时,KCl的溶解度为40g。40℃时,将50g KCl固体加入盛有100g水的烧杯中,充分溶解得到溶液。下列说法正确的是
A. 得到的是饱和溶液
B. 溶液的质量是150g
C. 溶液中溶质质量分数的计算式为 ![]()
D. 若再向烧杯中加入一定量水,此时溶液中溶质的质量分数一定减小
【答案】A
【解析】
40℃时,KCl的溶解度为40g。40℃时,将50g KCl固体加入盛有100g水的烧杯中,充分溶解得到溶液最多能溶解40g KCl。此时有10g KCl没有溶解,得到饱和溶液,溶液质量为140g,溶质的质量分数为:![]() 。
。
A、由分析可知,得到的是饱和溶液,说法正确,故符合题意;
B、溶液的质量是100g+40g=140g;说法错误,故不符合题意;
C、溶液中溶质质量分数的计算式为 ![]() ,说法错误,故不符合题意;
,说法错误,故不符合题意;
D、40℃时,将50g KCl固体加入盛有100g水的烧杯中,形成的是饱和溶液,固体未完全溶解,若再向烧杯中加入一定量水,此时溶液中溶质继续溶解,但是质量分数一定先不变,后再减小。说法错误,故不符合题意;
故选A

 通城学典默写能手系列答案
通城学典默写能手系列答案【题目】从A或B中任选一个作答。若均作答,按A计分。
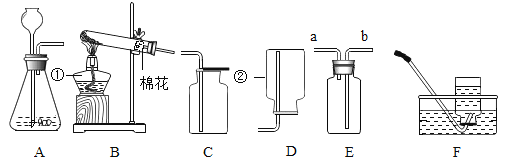
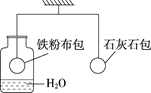
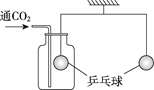
利用下图所示的装置完成实验(杠杆已经调至平衡)。
A | B |
放置较长一段时间后,左边铁粉布包______(填“上升”或“下降”),是因为铁粉与________发生了反应。 | 通入二氧化碳一段时间,左边乒乓球____(填“上升”或“下降”),再向集气瓶中滴入足量NaOH溶液,杠杆逐渐趋于平衡,发生反应的化学方程式为________。 |
|
|
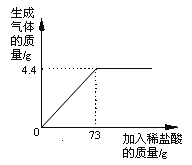
【题目】小苏打(主要成分为NaHCO3)中常含有少量氯化钠.化学小组的同学为了测定小苏打中NaHCO3的质量分数,进行了以下实验:将样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示.
物 质 | 样 品 | 消耗稀盐酸质量 | 反应后溶液质量 |
质量(g) | 9 | 75.4 | 80 |
计算:
(1)样品中的NaHCO3质量分数;
(2)所得溶液中溶质的质量分数.