题目内容
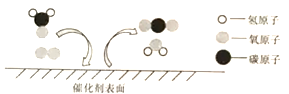
【题目】分析、归纳、推理是学习化学的重要方法,请同学们根据下面微观粒子反应(在水溶液中进行反应,水分子已省略)示意图,分析解决下列问题。
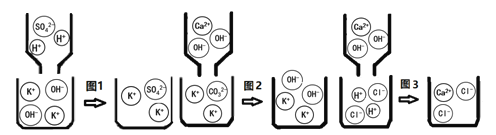
(1)图1所用到的稀硫酸是把10ml的浓硫酸和90ml的水混合而成的,但在混合后发现其体积少于100ml,试从微观角度分析其原因:__。
(2)图2发生反应的微观实质是Ca(OH)2溶液中的__(填化学用语)与K2CO3溶液中的(填化学用语)发生反应__;
(3)从图1、图2、图3可以发现,碱溶液中都含___(填化学用语),因此它们具有相似化学性质。试分析图1、图2、图3的反应中,属于碱的共同性质的是__。(填图序号)
(4)写出一种既能与氢氧化钙溶液又能与硝酸钙溶液反应的物质:____(填化学式)。
【答案】分子间存在间隔 Ca2+ CO32- OH-, 图1和图3(全对才给分) Na2CO3(合理可给分)
【解析】
图中氢氧化钾在溶液中会发生电离,电离出氢氧根离子、钾离子,硫酸在溶液中电离出硫酸根离子、氢离子,酸和碱发生反应是离子之间发生反应,复分解反应发生的条件是生成气体或沉淀或水。
(1)图1所用到的稀硫酸是把10mL的浓硫酸和90mL的水混合而成的,但在混合后发现其体积少于100mL,微观角度来看,是分子间存在间隔。
(2)图2发生反应的微观实质是Ca(OH)2溶液中的Ca2+和K2CO3溶液中的CO32-发生反应生成碳酸钙沉淀,符合复分解反应的条件。
(3)从图1、图2、图3可以发现,碱溶液中都含OH-,因此它们具有相似化学性质。图1、图2、图3的反应中,属于碱的共同性质的是图1和图3,都能和酸反应生成相应的盐和水。
(4)既能与氢氧化钙溶液又能与硝酸钙溶液反应的物质,必须要生成气体或沉淀,碳酸钠和氢氧化钙、硝酸钙都能反应生成碳酸钙沉淀,故化学式为Na2CO3。

 举一反三期末百分冲刺卷系列答案
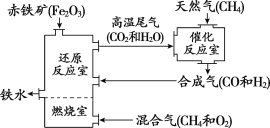
举一反三期末百分冲刺卷系列答案【题目】某化工厂用石灰石和铜屑等设计生产石青、波尔多液的工艺流程如下:
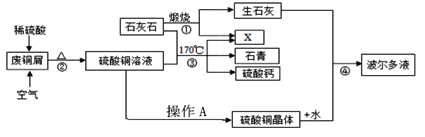
查阅资料:硫酸铜的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
溶解度/g | 14.3 | 17.4 | 20.7 | 25.0 | 28.5 | 33.3 | 40.0 | 55.0 | 75.4 |
(产品制备)
(1)流程图中X的化学式______
(2)反应②在80℃条件下制备硫酸铜,其化学方程式为_______。操作A将CuSO4溶液进行蒸发浓缩、________、过滤、洗涤等操作即得到硫酸铜晶体。
(组成测定)
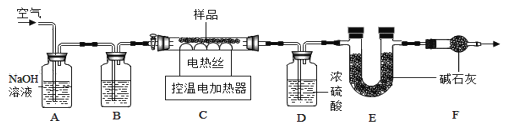
小组同学为测定石青的组成,称取了一定质量的石青样品,用如图装置进行实验。
查阅资料:
①石青的化学式可表示为aCuCO3b Cu(OH)2
②Cu(OH)2在66℃~68℃完全分解:Cu(OH)2![]() CuO+H2O; CuCO3在200℃~220℃完全分解:CuCO3
CuO+H2O; CuCO3在200℃~220℃完全分解:CuCO3![]() CuO+CO2↑
CuO+CO2↑
③ CuSO4固体为白色,CuSO45H2O固体为蓝色
实验步骤:①连接仪器,并_________, 准确称取69.2g aCuCO3bCu(OH)2放在C装置中;②打开活塞鼓入一段时间空气,称量装置D、E的质量;③关闭活塞,控制C装置中的温度为250℃对石青进行热分解,直至C装置中剩余固体质量不再变化为止;④打开活塞,_______;⑤冷却后,称量,装置D增重3.6g,装置
(3)完善上述实验步骤中的填空:①_______;④_____________。
(4)洗气瓶A中氢氧化钠溶液的作用是______;B中所装液体为____(填名称)。
(5)试确定石青的化学式______(请写出计算过程)。
(6)若缺少F装置,测得的a:b的值将________(选填“偏大”、“偏小”、“不变”)。
(脱水探究)
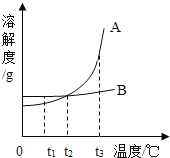
硫酸铜晶体受热会逐步失去结晶水。取纯净的CuSO45H2O固体2.50g,放在上图实验装置C中进行加热,测定固体质量随温度的变化情况如图所示。
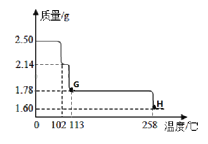
(7)G点固体的化学式是________;H点固体的颜色是_______。
(8)将CuSO45H2O固体加热到570℃分解后,得到的主要产物是黑色粉末、硫的一种氧化物和水蒸气,该反应的化学方程式为:_________。