题目内容
【题目】分析处理图表中的信息是学习化学的种重要方法。
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①.30℃时,KNO3溶液的最大浓度(溶质质量分数)为________(只列计算式,不需要计算结果).
②.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是_____。
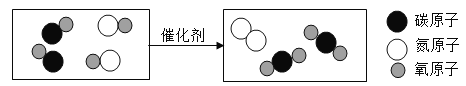
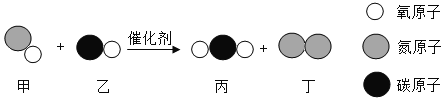
(2)根据电解水的实验,回答下列问题:
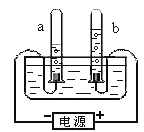
①.从宏观上观察:图示a、b管中产生的体积比约为2:1,则他们的质量比为_________。
②.从微观上分析:下列说法错误的是_________(填字母)。
A.水是由水分子构成的
B.水是由氢原子和氧原子构成的
C.每个水分子是由2个氢原子和1个氧原子构成的
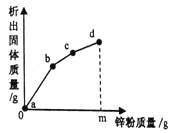
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答。
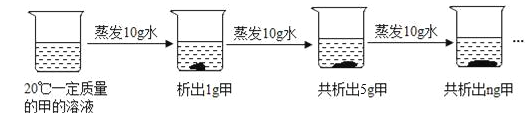
①蒸发前原溶液是_______(填“饱和”或“不饱和”)溶液,n的数值是______。
②依据上述实验,你认为甲的溶解度随温度变化的趋势是________(填序号)。
A.随温度升高而增大 B随温度升高面减小 C无法判断。
【答案】![]() ×100% 36~36.3 1:8 B 不饱和 9 C
×100% 36~36.3 1:8 B 不饱和 9 C
【解析】
(1)下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
①.30℃时,KNO3溶液的最大浓度(溶质质量分数)为是饱和溶液的溶质质量分数,为![]() ;
;
②.根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36~36.3;
(2)根据电解水的实验,回答下列问题:①.从宏观上观察:图示a、b管中产生的体积比约为2:1,反应方程式为,2H2O ![]() 2H2↑+ O2↑,由方程式可知生成氢气和氧气的质量比为1:8;
2H2↑+ O2↑,由方程式可知生成氢气和氧气的质量比为1:8;
②.从微观上分析:
A.水是由水分子构成的,选项说法正确;
B.水分子是由氢原子和氧原子构成的,选项说法错误;
C.每个水分子是由2个氢原子和1个氧原子构成的,选项说法正确;故选B;
(3)①.由题中信息可知,第一次蒸发10g水不饱和溶液,第三次还是蒸发饱和溶液中10g水,析出晶体应该是4g,n的数值是9;
②.上述实验是在恒温条件下进行的,不能判断甲的溶解度随温度变化的趋势故选C。

 名校课堂系列答案
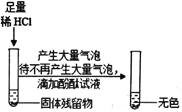
名校课堂系列答案【题目】工业上用高温煅烧石灰石制备CO2,某探究小组欲探究煅烧后的固体残留物成分
[资料] ①CaO +2HCl = CaCl2+ H2O ②CaCl2溶液呈中性
(1)高温煅烧石灰石的方程式为___________________,根据化学方程式进行猜想:
猜想一:只有CaO,猜想二:有 CaO和________________
[实验验证]
(2)两位同学设计实验方案如下表
甲同学 方案一 | 乙同学 方案二 | |
实验步骤现象 |
|
|
①据甲同学方案一中现象,可判断剩余固体中一定含有_______,用方程式解释__________。
②乙同学认为猜想二一定正确,该同学的方案是否合理?_______,理由是______________。
③丙同学认为结合方案一和方案二可以判定猜想二成立,该观点____(填“正确”或“不正确”)
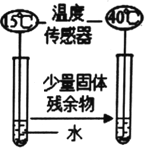
[讨论与反思]小组同学认为,导致残余固体中不止含有一种物质的原因可能是石灰石的状态导致的,为此他们模拟工业操作,在实验室高温煅烧石灰石,相关记录如下表
石灰石(不含杂质) | 状态 | 温度 | 最终收集到CO2的质量 | |
实验1 | 2g | 块状 | 800℃ | 0.748g |
实验2 | 未知 | 粉末状 | 800℃ | 0.876g |
(3)上表中实验1中的产率为___________(产率=实际产物质量÷理论产物质量×100%),为了达成实验目的,实验2中未知质量应该是__________g,
[反思总结]
(4)从表中数据可知,高温煅烧石灰石最好选择_______状态反应更充分,理由是________。