题目内容
【题目】某校化学兴趣小组就空气中氧气的含量进行实验探究:(9分)
[集体讨论]:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(填编号) 。
A.蜡烛 B.红磷 C.硫粉
为了充分消耗容器中的氧气,药品的用量应保证 。

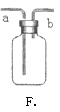
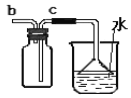
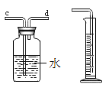
(2)小组同学共同设计了如下图的两套装置, 你认为合理的是(填编号) 。
为了确保实验的成功,在装药品之前应该 。
[分组实验] 在讨论的基础上,他们分组进行了实验。
[数据分析] 实验结束后,整理数据如下:(注:集气瓶容积为100mL)
组 别 | 1 | 2 | 3 | 4 | 5 | 6 |
进入集气瓶中水的体积(mL) | 20 | 21 | 14 | 20 | 28 | 19 |
(3)根据燃烧红磷测定空气中氧气含量的实验原理是 。
[分组讨论]
(4)第三组同学进入集气瓶中水的体积明显比其他组同学少,原因是 (答一条)
第五组同学进入集气瓶中水的体积明显比其他组同学多,原因是 (答一条)
(5)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。
[实验总结]
(6)小组的同学反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择或生成物的要求上应考虑的是 。
【答案】(1)B 足量(2)A 检查装置气密性
(3)红磷燃烧消耗氧气,生成固体,使容器内体积减小、压强减小
(4)红磷的量太少、装置漏气等
弹簧夹没有夹紧或点燃红磷伸入瓶中没有立即塞紧瓶塞
(5)五分之一
(6)易燃烧,生成物为固体只与空气中的氧气反应
【解析】
试题分析:(1)蜡烛和硫粉与氧气反应,生成物中有气体,不能准确测定空气中氧气的含量,只有红磷在空气中与氧气反生成固体物质,不影响空气成份的测定,故选B;也只有红磷足量或过量,才能完全消耗集气瓶中的氧气;
(2)为了保证红磷与空气中的氧气充分反应,应将红磷伸到集气瓶的中下部,故A装置更合理;而为了保证实验成功,在装药品之前要先检查装置的气密性。
(3)用燃烧红磷测定空气中氧气含量的实验原理是:红磷燃烧消耗氧气,生成固体,使容器内体积减小、 压强减小,水就会沿导管进入集气瓶,进入集气瓶中水的体积就等于消耗的氧气的体积。
(4)因为氧气约占空气体积的五分之一,故理论上进入的水的体积大约等于空气体积的五分之一。进入集气瓶中水的体积偏小可能由于红磷量不足,没有消耗完瓶中氧气,或装置漏气等。进入集气瓶中水的体积偏大可能是由于弹簧夹没有夹紧或点燃红磷伸入瓶中没有立即塞紧瓶塞。
(5)分析表格中数据可知,大多数同学都验证出氧气约占空气体积的五分之一。
(6)用燃烧法测定空气中氧气含量的实验时,应选择易燃烧,且只与空气中的氧气反应,并且生成物为固体的物质。