题目内容
【题目】一包固体粉末可能含有NaNO3、CaCO3、NaOH、FeCl3、NaCl和Ba(NO3)2中的一种或几种,为确定其组成,现做如下实验:取少量固体加足量的水溶解,过滤得沉淀I和无色溶液I,后续实验及现象如图:
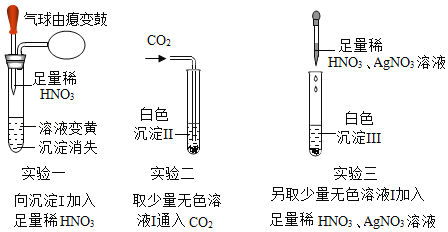
(1)写出实验一中,使溶液变黄的反应化学方程式___。
(2)白色沉淀Ⅱ是___(填化学式)。
(3)通过上述实验,固体粉末中不能确认是否存在的物质是___。
【答案】Fe(OH)3+3HNO3=Fe(NO3)3+3H2O BaCO3 NaNO3、NaCl
【解析】
取少量固体加足量的水溶解,过滤得沉淀Ⅰ和无色溶液Ⅰ;向沉淀Ⅰ加足量的硝酸,溶液变黄,说明沉淀中含有氢氧化铁,气球变大,说明沉淀中含有碳酸钙,从而说明原固体中含有碳酸钙、氢氧化钠和氯化铁;溶液中通入二氧化碳产生白色沉淀,说明此时的溶液中含有氢氧化钠和硝酸钡,产生的沉淀是碳酸钡沉淀;向无色溶液中加入硝酸和硝酸银有沉淀产生,由于氢氧化钠和氯化铁会反应生成氯化钠,因此不能确定原固体中氯化钠的存在,根据整个实验现象,也不能确定硝酸钠的存在。
(l)氢氧化铁和稀硝酸反应生成硝酸铁和水,化学方程式为:Fe(OH)3+3HNO3=Fe(NO3)3+3H2O;
(2)根据以上分析可知:白色沉淀Ⅱ是BaCO3;
(3)通过上述实验,固体粉末中不能确认是否存在的物质是:NaNO3、NaCl。

【题目】活动小组为测定由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该固体混合物各20g,分别缓慢加入到50 g、100 g、150 g某稀硫酸中,测得三组实验数据如下表:
组别 | 第1组 | 第2组 | 第3组 |
稀硫酸质量/g | 50 | 100 | 150 |
剩余固体的质量/g | 10.0 | 4.0 | 4.0 |
根据实验及有关数据进行分析与计算:
(1)第1组实验中_____________(填“氧化铜”“稀硫酸”或“氧化铜与稀硫酸”)完全反应。
(2)样品中氧化铜的质量分数是__________g。
(3)根据第1组实验数据计算所用的稀硫酸溶质的质量分数__________(写出计算过程)。
(4)若将第2组实验后的混合物过滤,在滤液中滴加10%的NaOH溶液,请画出在该混合溶液中加入10% NaOH溶液的质量与生成沉淀质量变化关系的曲线图__________。