题目内容
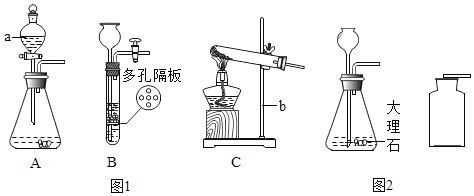
【题目】请同学们搭乘“化学地铁”一起畅游物质世界吧!如下图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。“2~5号站”各站的对应物质属于不同类别的纯净物。
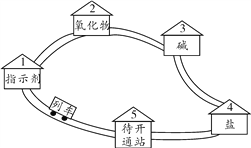
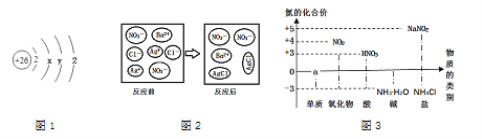
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变__________色。
②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠的化学方程式为____________________________。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为___(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为____________ (写一个)。
③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为__________(写一种物质),“稀盐酸”列车方能走完。
【答案】 蓝 Na2CO3+H2O+CO2==2NaHCO3 AgNO3 Fe+2HCl==FeCl2+H2↑ CuO
【解析】(1)若列车上的物质为“碳酸钠溶液”。 ①碳酸钠溶液呈碱性,紫色石蕊遇碱变蓝,列车途经“1号站”时,若指示剂为紫色石蕊溶液,溶液变蓝色。②列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠的化学方程式为Na2CO3+H2O+CO2=2NaHCO3。(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为AgNO3,AgNO3 与盐酸反应生成氯化银白色沉淀,与碳酸钠溶液反应生成碳酸银白色沉淀。②“稀盐酸”列车途经“5号站”时,反应的化学方程式为Fe+2HCl=FeCl2+H2↑。③“稀盐酸”列车途经“1、2、3号站”时,原“碳酸钠溶液”列车途经某站的对应物质必须更换为CuO,CuO与盐酸反应生成氯化铜和水。
点睛∶AgNO3 与盐酸反应生成氯化银白色沉淀,与碳酸钠溶液反应生成碳酸银白色沉淀。碳酸钠溶液呈碱性,石蕊遇酸变红,遇碱变蓝。

【题目】(1)某兴趣小组准备通过锌与稀硫酸反应产生的氢气来测定稀硫酸中溶质的质量分数,装置如下:
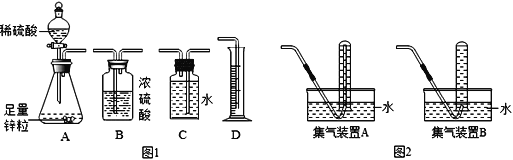
①小明同学用如图1所示装置进行实验,你认为他应该选择的最简易的装置及其连接顺序是:A→______→ D。
②小明若用图2装置收集氢气,应选择集气装置____(填“A”或“B”),为保证测量结果的准确性,收集气体的时机是_________。
a.导管口还没有气泡产生时
b.导管口连续均匀冒出气泡时
c.导管口冒出气泡很多时
③小张同学用如图3所示装置进行了实验:
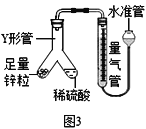
Ⅰ.下列能说明装置气密性良好的是_________。
A.连接仪器后,向水准管中注水,直至左右两边管内形成稳定高度差。
B.向水准管内注水,连接好左侧装置,抬高水准管,左右两边液面始终相平。
Ⅱ.反应完毕后,每间隔1分钟读取气体体积、气体体积逐渐减小,直至体积不变。气体体积逐渐减小的原因是_________________(排除仪器和实验操作的影响因素)。
Ⅲ.若实验中测得稀硫酸的溶质质量分数偏大,下列可能的原因是____________。
a.装置漏气 b.读取数据时水准管的水面高于量气管的水面
c.未待冷却就读取量气管读数
(2)在金属活动性顺序表中,排在前面的金属能把位于后面的金属从它的盐溶液中置换出来,但小明在做金属钠与硫酸铜溶液反应的实验时,却出现了异常现象。
【进行实验】取一块绿豆大小的金属钠,放入盛有20毫升硫酸铜溶液的小烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,一会儿部分沉淀渐渐变黑,将反应后烧杯中的混合物进行过滤,得滤渣和无色滤液。
【提出问题】①生成的气体是什么?
②滤渣的成分是什么?
③无色滤液中的溶质是什么?
【查阅资料】①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60~80℃变暗,温度再高分解为相应的金属氧化物(化合价不变)和水。
【实验探究一】 探究生成的气体是什么?
小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,把气体通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。说明生成的气体是___________。
【实验探究二】 探究滤渣的成分是什么?
【猜想假设】滤渣中含有Cu(OH)2和_____________,还可能含有Cu。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量滤渣,向其中加入足量的稀硫酸 | ____________________ | 滤渣中没有Cu |
【实验结论】通过实验,小明同学得出结论:钠加入到硫酸铜溶液中会先与水反应,生成物再与硫酸铜反应生成氢氧化铜。请写出上述发生的两个反应的化学方程式______________ ,________________。
【实验探究三】探究无色滤液的溶质是什么?
【猜想假设】猜想① Na2SO4 , 猜想②________________。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量无色滤液,向其中加入__________ | 无明显变化 | 猜想①成立 |
【反思交流】钠加入硫酸铜溶液中出现黑色物质的可能原因是(用化学方程式表示)_________。
【题目】某校兴趣小组同学准备进行常见酸、碱、盐的性质实验时,发现实验台上摆放的药品中,有一装溶液的试剂瓶未盖瓶盖且标签破损(如下图),于是决定对这瓶溶液进行实验探究:

【提出问题】这瓶溶液是什么溶液?
【获得信息】酸、碱、盐的性质实验中常用到含有钠元素的物质是氯化钠、氢氧化钠、碳酸钠
【提出猜想】这瓶溶液是:猜想一:氯化钠溶液;猜想二:氢氧化钠溶液; 猜想三:碳酸钠溶液。
【实验推断】
⑴丽丽取样滴加无色酚酞试液,溶液呈红色,得出结论:该溶液不可能是___________溶液,理由是______________。
⑵芳芳另取样滴加稀盐酸有_______产生,反应的化学方程式为_______________,芳芳得出结论:该溶液是碳酸钠溶液。
⑶小明看到露置在空气中未盖的试剂瓶,认真进行了思考,他认为芳芳的结论不完全正确,该溶液也可能是氢氧化钠溶液,理由是_____________________________。(写出化学方程式)
同学们讨论后一致认为小明的结论需要通过实验进行验证:
【查阅资料】氯化钙溶液呈中性
【设计实验】同学们讨论后又设计了如下实验:
实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
①取少量溶液于试管中,滴加足量的氯化钙溶液,并不断振荡。 | 有白色沉淀产生。 | 溶液中含有碳酸钠。 |
②将①的试管静置后,取上层清液向其中滴加____________。 | 发现 _________ | 溶液中还含有氢氧化钠 |
【实验结论】小明的结论是正确的。
【探究启示】实验取完药品后应_________________。