题目内容
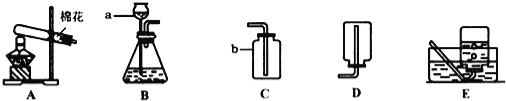
【题目】如图,A、B、C、D是四种粒子的结构示意图,E是铈元素在元素周期表中的信息。
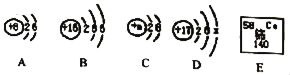
(1)若D为原子,则D中x的值为______;
(2)写出A、B两粒子对应的元素形成化合物的化学式______;
(3)根据E中提供的信息,可知铈原子的中子数为______;
(4)C粒子中,若m>10,则阳离子的符号可能为______(至少写一种)
【答案】7 SO2 82 Al3+、Mg2+、Na+
【解析】
元素周期表中,每种元素占据的空格中,左上角是原子序数,右上角是元素符号,中间是元素名称,下面是相对原子质量;
原子中,核电荷数=核内质子数=核外电子数=原子序数;
相对原子质量≈质子数+中子数,单位不是g;
化合物中元素化合价代数和为零;
一般情况下,最外层电子数小于4的,反应中容易失去电子,大于4的反应中容易得到电子,等于4的,既不容易得到电子,也不容易失去电子,因此最外层电子数相等的元素化学性质相似,最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。
(1)若D为原子,则D中x的值为:17﹣2﹣8=7,
故填:7。
(2)写出A(氧元素)、B(硫元素)两粒子对应的元素形成化合物是二氧化硫,二氧化硫的化学式是SO2,
故填:SO2。
(3)根据E中提供的信息,可知铈原子的中子数为:140﹣58=82,
故填:82。
(4)C粒子中,若m>10,则阳离子的符号可能为带3个单位正电荷的铝离子,或带2个单位正电荷的镁离子,或带1个单位正电荷的钠离子。
故填:Al3+、Mg2+、Na+。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案【题目】“五一”假期,小兵对“锌与硫酸反应快慢的影响因素”进行了探究。
【提出问题】锌与硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a.可能与硫酸的质量分数有关;
b.可能与锌的形状有关。
【设计并实验】小兵用不同质量分数的硫酸和不同形状的锌进行如下实验。
实验 编号 | 硫酸的质量 分数(均取 20 mL) | 锌的形状 (均取1 g) | 氢气的体积(mL) (均收集3分钟) |
① | 20% | 锌粒 | 31.7 |
② | 20% | 锌片 | 50.9 |
③ | 30% | 锌粒 | 61.7 |
④ | 30% | 锌片 | 79.9 |
(1)写出稀硫酸与锌反应的化学方程式:________________________。
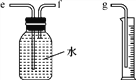
(2)小兵用如图所示装置收集并测量氢气的体积,其中量筒的作用是________________________________________,氢气应从________(填“e”“f”或“g”)管通入。
【收集证据】(3)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是____________。
【得出结论】(4)结论是________________________________________________________________。
(5)下表是小兵第①组实验的详细数据。
时段(均 为1分钟) | 第1 分钟 | 第2 分钟 | 第3 分钟 | 第4 分钟 | 第5 分钟 | 第6 分钟 |
H2的体积 | 3.1 mL | 16.7 mL | 11.9 mL | 9.6 mL | 7.6 mL | 6.0 mL |
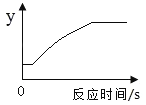
请描述锌与硫酸反应的快慢的变化并解释原因:______________________________。
(6)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证。___________________。