题目内容
【题目】实验是进行科学探究的重要手段。请回答下列问题。
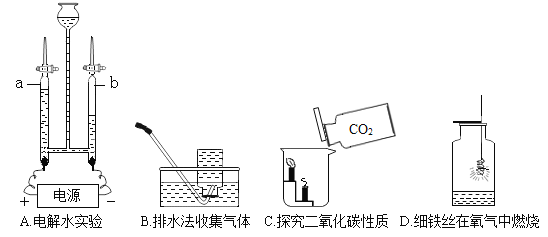
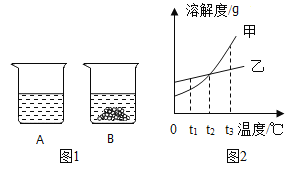
(1)实验A发生反应的化学方程式是_____。当电源接通一段时间后,a管与b管中气体的体积比约为_____。
(2)实验B集气瓶内要装满水的目的是_____,某气体不能用该方法收集,说明该气体具有_____的性质。
(3)实验C中观察到的现象是_____,说明二氧化碳具有的性质是_____、不支持燃烧、不能燃烧。
(4)实验D中水的作用是_____。
【答案】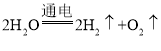 1:2 收集气体更纯 能溶于水 蜡烛由下而上依次熄灭 密度比空气大 防止高温熔融物炸裂集气瓶
1:2 收集气体更纯 能溶于水 蜡烛由下而上依次熄灭 密度比空气大 防止高温熔融物炸裂集气瓶
【解析】
(1)实验A,电解水时生成氧气和氢气,对应的化学方程式为: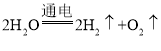 ,电解水的实验中正氧负氢氢二氧一,由于玻璃管a与正极相连,所以产生的气体是氧气,当电源接通一段时间后,a管与b管中气体的体积之比也就是氧气和氢气的体积比为 1:2;由此得出的实验结论是水是由氢、氧元素组成的。
,电解水的实验中正氧负氢氢二氧一,由于玻璃管a与正极相连,所以产生的气体是氧气,当电源接通一段时间后,a管与b管中气体的体积之比也就是氧气和氢气的体积比为 1:2;由此得出的实验结论是水是由氢、氧元素组成的。
(2)实验B利用排水法收集气体,集气瓶内装满水的目的是排出集气瓶中的空气,使收集气体更纯;某气体不能用该方法收集,说明该气体能溶于水;
(3)二氧化碳密度比空气大,不助燃,不可燃,所以观察到的现象是烧杯中位于低处的蜡烛先熄灭,位于高处的蜡烛后熄灭,因此二氧化碳可用于灭火;
(4)由于铁丝在氧气中燃烧生成高温的熔融物四氧化三铁,所以实验D中水的作用是防止高温熔融物炸裂集气瓶。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】取20g碳酸钠和碳酸氢钠的固体混合物,加热至不再产生气体2NaHCO3![]() Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
Na2CO3+H2O+CO2↑),使生成的水完全被浓硫酸吸收,测得加热时间和浓硫酸质量增加的关系如表:
时间 | 0分钟 | 1分钟 | 2分钟 | 3分钟 |
仪器和浓硫酸的质量总和(g) | 150 | 150.9 | 151.8 | 151.8 |
(1)当完全反应后,生成水的质量为_____g。
(2)计算混合物中碳酸氢钠的质量分数________。(要求写出计算过程)
(3)将上述混合物完全分解后的固体溶解于186.2g 水中,待固体完全溶解后所得溶液中溶质的质量分数为_____。