题目内容
请根据下图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:(CaCl2溶于水,但不与稀盐酸反应)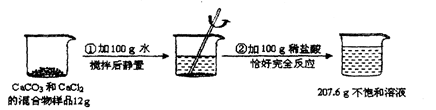
计算原混合物样品中CaCl2的质量(写出计算过程)。
2g
解析试题分析:实验过程中产生二氧化碳的质量=100g+100g+12g-207.6g=4.4g;设原混合物中碳酸钙的质量为x,则: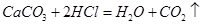
100 44
x 4.4g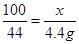
x=10g
故原混合物中氯化钙的质量=12g-10g=2g。
考点:根据化学方程式的计算。

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
“黄铜”是铜、锌合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下:(烧杯质量均为56g)
| | 甲 | 乙 | 丙 |
| 烧杯+稀盐酸质量 | 139g | 129g | 129g |
| 加入黄铜样品质量 | 20g | 24g | 20g |
| 充分反应后,烧杯+剩余物质质量 | 158.8g | 152.8g | 148.8g |
请回答下列问题:
(1) 同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是 。
(2)计算黄铜样品中锌的质量分数。
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 15.05 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 3.03 |
| ③ | 30 | 5 | 35 | | 2 | 48.21 |
| ④ | 30 | 5 | 55 | | 2 | 10.95 |
(1)通过实验①和②对比可知,化学反应快慢与 有关;
(2)通过对比实验③和 可知,化学反应快慢与温度的关系是 。
(3)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是
某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成,取四份样品分别加稀硫酸反应,其实验数据记录如下表。
| 样品 | 第1份 | 第2份 | 第3份 | 第4份 |
| 取样品质量(g) | 50.0 | 50.0 | 50.0 | 50.0 |
| 取稀硫酸质量(g) | 40.0 | 80.0 | 120.0 | 160.0 |
| 产生气体质量(g) | 0.4 | 0.8 | 1.0 | 1.0 |
试计算:
⑴根据测得的数据分析,第1份样品中 (填物质)完全反应了。
⑵列式计算黄铜屑样品中的锌的质量分数。
⑶请在图中画出在50.0g样品中加稀硫酸的质量与产生气体质量变化关系的示意图。