题目内容
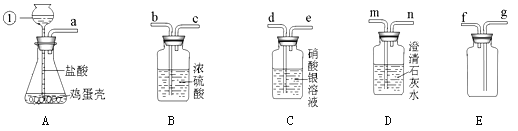
【题目】氢氧化钠和氢氧化钙是两种常见的碱。李晓同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的三组实验:
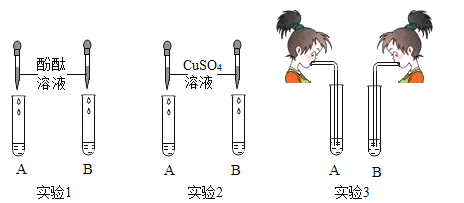
(1)实验l中,两支试管的溶液都变成______色。
(2)实验2中,若B盛装的是NaOH溶液,发生反应的化学方程式为______。
(3)实验3中,李晓同学向两支试管吹气,A中有白色沉淀生成,B中无现象,为了探究吹气后B中溶质的成分,李红进行了如下探究。
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
实验和结论:
实验 | 实验现象 | 结论 |
取B中少量溶液,加人澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液。 | ______ | 猜想3成立 |
反思与评价:
老师评价李晓得出的结论不正确,是因为猜想______(填数字)也会产生相同的现象,如果要验证“猜想3成立”,必须要换试剂,将Ca(OH)2换成______溶液。
【答案】红 CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 先产生白色沉淀,后溶液变红色 2 氯化钙
【解析】
氢氧化钙溶液和氢氧化钠溶液都是显碱性溶液,都能使酚酞试液变红色;二氧化碳和氢氧化钙反应生成白色沉淀碳酸钙和水,和氢氧化钠反应生成碳酸钠和水;碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,和氯化钙反应生成碳酸钙沉淀和氯化钠。
(1)实验l中,两支试管的溶液都变成红色,这是因为氢氧化钙溶液和氢氧化钠溶液都是显碱性,都能使无色酚酞溶液变红。 故填:红。
(2)实验2中,若B盛装的是NaOH溶液,氢氧化钠和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠,发生反应的化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。
故填:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4。
(3)取B中少量溶液,加人澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液,先产生白色沉淀,后溶液变红色,实验过程如下所示:
实验 | 实验现象 | 结论 |
取B中少量溶液,加人澄清石灰 水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液。 | 先产生白色沉淀,后溶液变红色 | 猜想3成立 |
反思与评价:
老师评价李晓得出的结论不正确,是因为猜想2也会产生相同的现象,这是因为碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠溶液显碱性,也能使酚酞试液变红色;
如果要验证“猜想3成立”,必须要换试剂,将Ca(OH)2换成显中性的氯化钙溶液,能够防止反应生成氢氧化钠影响实验结果。 故填:2;氯化钙。

【题目】如表是KCl和KNO3在不同温度下的溶解度.
温度/℃ | 20 | 30 | 40 | 50 | |
溶解度(g/100g水) | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
KNO3 | 31.6 | 45.8 | 63.9 | 85.5 | |
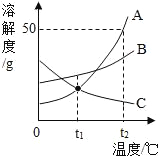
(1)硝酸钾的溶解度随温度的升高而_____(填“增大”或“减小”).
(2)用同一种方法可以使KCl、KNO3二种物质的溶液都析出晶体,该方法是_____.
(3)KCl、KNO3两种物质溶解度相等的温度在_____之间(用编号表示).
A 20℃以下 B 20℃~30℃ C 30℃~40℃ D 40℃~50℃
(4)20℃时,100g水中最多可溶解KCl的质量为_____;40℃时,将70gKCl的饱和溶液稀释成质量分数为20%的溶液,需加水_____g.
(5)将某温度下热的硝酸钾饱和溶液逐渐冷却至室温,下列有关量随时间变化趋势的图象不正确的是_____(用编号表示).