��Ŀ����
����Ŀ��ij��ѧ����Χ�ơ�����кͷ�Ӧ������ѧ���ֳ�����С�飬����ʦ�����¿�չ̽����������ǽ�ѧƬ�Σ��������ѧϰ��������д�ո������пո���
����ʾʵ�顿��һ������ϡH2SO4���뵽ʢ��NaOH��Һ��С�ձ�����
��ѧ�����ݡ��÷�Ӧ�Ļ�ѧ����ʽ ��
��������⡿ʵ����δ�۲쵽����������ͬѧ���������ʣ���Ӧ����Һ��������ʲô��
��������롿������ʣ���ҷ�������룮����ͬѧ�IJ������£����㲹�ϲ�������
����һ��ֻ��Na2SO4
���������Na2SO4��H2SO4
����������Na2SO4��H2SO4��NaOH
�����ģ�
����ͬѧ�����ϲ���������ɣ���Ϊ��һ�ֲ����Dz������ģ��������IJ����� ��
������ ��
��ʵ��̽����
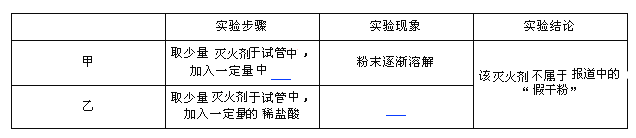
��1������ͬѧȡ�ձ��е���Һ�������Թ��У��μӼ���CuSO4��Һ�������Ա仯����Һ��һ��û�� ��
��2��Ϊ����֤������룬��ѧϰС�������ձ��е���Һ����ѡ������ʦ�ṩ��pH��ֽ��Na2CO3��Һ��BaC12��Һ��������������������̽����
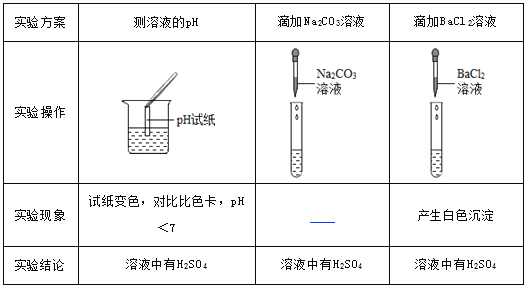
���ó����ۡ�ͨ��̽����ȫ��ͬѧһ��ȷ�����������ȷ�ģ�
�����۷�˼����ʦ��ͬѧ�����ö��ַ�������̽�������ҵó���ȷ���۸����˿϶���ͬʱָ����2���д����������Դ������ҷ�˼��ͬѧ�Ǿ�����˼������������������
��ʵ������еĴ����� ��
��ʵ�鷽����Ҳ��һ���Ǵ���ģ������ԭ���� ��
���𰸡���ѧ�����ݡ�H2SO4+2NaOH=Na2SO4+2H2O
��������롿��Na2SO4��NaOH ������ H2SO4��NaOH����Һ�в��ܹ���
��ʵ��̽������1��NaOH ��2�������ݲ���
�����۷�˼���� pH��ֽ������Һ��
��Na2SO4��BaCl2��ӦҲ�����ɰ�ɫ����������֤��һ����H2SO4����
��������
�����������ѧ�����ݡ�ϡH2SO4��NaOH��Һ��Ӧ�Ļ�ѧ����ʽΪ��H2SO4+2NaOH=Na2SO4+2H2O
��������롿�Է�Ӧ����Һ�����ʵ��жϣ���Ӧ��������һ���У���Ӧ������У����ܹ��������ʸ��������������룬�����ģ���Na2SO4��NaOH����һ�ֲ����Dz������ģ��������IJ����ǣ��������������ǣ�H2SO4��NaOH����Һ�в��ܹ���
��ʵ��̽������1������NaOH�Ļ�ѧ���ʣ�����CuSO4��Һ��Ӧ����������ͭ��ɫ�������ʱ���ͬѧȡ�ձ��е���Һ�������Թ��У��μӼ���CuSO4��Һ�������Ա仯����Һ��һ��û��NaOH
��2����������ķ�����̽�����ų��˲��������ģ�����ֻ��ȷ������һ�������������ߵ����������Ƿ������ᣬ�ʸ�������Ļ�ѧ���ʣ�������������Һ��Ӧ�������������̼����ʵ�鷽��2������ �ǣ������ݲ���
�����۷�˼����ʵ������еĴ����ǣ�����ֱ�ӽ�pH��ֽ������Һ������Ӧ�ò�����պȡ����Һ����PH��ֽ��
��ʵ�鷽����Ҳ��һ���Ǵ���ģ����������������ԭ����Na2SO4��BaCl2��ӦҲ�����ɰ�ɫ����������֤��һ����H2SO4����