题目内容
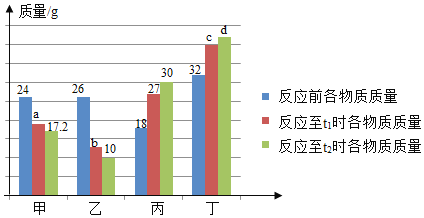
【题目】在密闭容器内进行某化学反应,测量反应前(t0)、反应中(t1)、反应后(t2)三个时刻甲乙丙丁4种物质的质量分数,得到质量分数分布图分别如下:
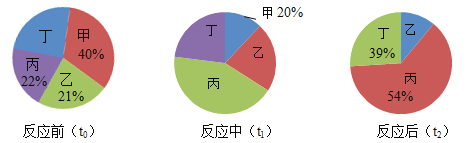
下列说法错误的是( )
A. 该反应中,乙是反应物,丁是生成物
B. t1时刻,甲和乙的质量比为5:7
C. 若丙是Cu,丁是二氧化碳,则甲、乙的化学计量数之比为2:1
D. 若反应前物质总质量为100克,如果再增加20g甲,则甲与乙可恰好完全反应
【答案】BC
【解析】
由反应前(t0)可知,丁的质量分数=1-21%-22%-40%=17%。由反应后(t2)可知,乙的质量分数=1-54%-39%=7%,甲的质量分数为0。参加反应的甲、乙、丙、丁的质量比为40%:(21%-7%):(54%-22%):(39%-17%)=20:7:16:11。由图可知,甲、乙质量分数减小,属于反应物,丙、丁质量分数增大,属于生成物。
A、由分析知,该反应中,乙是反应物,丁是生成物,正确,不符合题意;
B、由图可知,t1时刻,甲反应了二分之一,故乙消耗的质量分数为(21%-7%)×![]() =7%,故t1时刻,甲和乙的质量比为20%:(21%-7%)=10:7,错误,符合题意;
=7%,故t1时刻,甲和乙的质量比为20%:(21%-7%)=10:7,错误,符合题意;
C、若为碳还原氧化铜,则 ,160:12≠20:7,质量比不符合;若为一氧化碳还原氧化铜,则
,160:12≠20:7,质量比不符合;若为一氧化碳还原氧化铜,则![]() ,80:28 =20:7,质量比符合要求。但此时甲、乙的化学计量数之比为1:1,错误,符合题意;
,80:28 =20:7,质量比符合要求。但此时甲、乙的化学计量数之比为1:1,错误,符合题意;
D、若反应前物质总质量为100克,则甲的质量为40g,乙的质量为21g,再增加20g甲,则反应前甲、乙质量比为(40g+20g):21g=20:7,所以甲与乙可恰好完全反应,正确,不符合题意。故选BC。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】在密闭容器内有氧气、二氧化碳、水蒸气和一种未知物质W,在一定条件下充分反应,测得反应前后各物质的质量如表所示,则下列说法中正确的是( )
物质 | 氧气 | 二氧化碳 | 水蒸气 | W |
反应前质量/g | 50 | 1 | 1 | 23 |
反应后质量/g | 2 | 45 | 28 | x |
A. 根据质量守恒定律,x的值应为2
B. 该反应属于置换反应
C. 该反应中的二氧化碳和水蒸气的质量比为44:27
D. 该反应中物质W含碳元素的质量为10g
【题目】下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | ||||||
Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
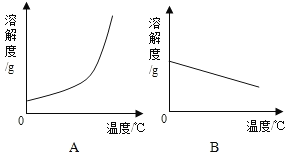
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”).
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有_____(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水 ⑤加入氢氧化钙
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲_____乙(填“>”“<”或“=”).