题目内容
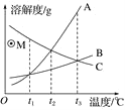
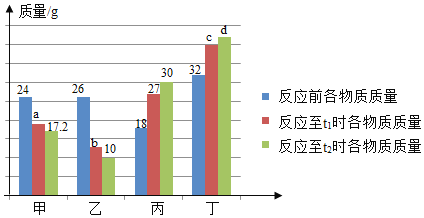
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量。下列说法正确的是( )
A. b的数值为14
B. 该反应为复分解反应
C. 反应过程中乙与丁发生改变的质量比为5:6
D. 充分反应后生成丙的质量为37.5g
【答案】A
【解析】
化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和,是因为化学反应前后,元素的种类不变,原子的种类、总个数不变。
A、根据题意有:(26﹣b):(27﹣18)=(26﹣10):(30﹣18),b=14,选项说法正确;故符合题意;
B、反应后甲、乙质量减小,是反应物,丙丁质量增大,是生成物,但是不能判断各种物质的种类,即不能判断是单质还是化合物,因此反应不一定是复分解反应,选项说法不正确;故不符合题意;
C、d=24+26+18+32﹣17.2﹣10﹣30=42.8,反应过程中乙与丁发生改变的质量比为:(26﹣10):(42.8﹣32)=40:27,选项说法不正确;故不符合题意;
D、由图中数据可知,充分反应后生成丙的质量为:30g﹣18g=12g,选项说法不正确;故不符合题意;
故选A

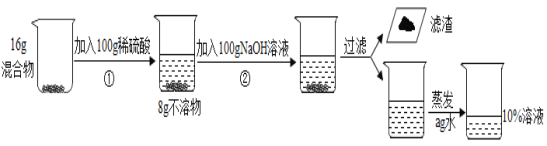
【题目】(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?其催化效果如何?
(实验探究)
实验步骤 | 实验现象 |
I.分别量取5mL5%过氧化氢溶液放入A、B 两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象。 |
II.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次试验,观察现象。 | 试管中均产生气泡,带火星木条均复燃 |
III.将实验II中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag。 | |
IV分别量取5mL5%过氧化氢溶液放入C、D 两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象。 |
(实验结论)
(1)实验I证明:氧化铁_____(“能”或“否”)改变过氧化氢分解反应的速率;
(2)实验II、III证明:氧化铁的_____和_____在反应前后均没有发生变化,可以作过氧化氢分解的_____;
(3)写出氧化铁催化过氧化氢分解的符号表达式_____。
(实验评价)(1)实验设计IV的目的是_____;
(2)若实验IV观察到D试管中产生气泡的速率更快,由此你可以得到的结论是_____。
(3)在催化剂相同条件下,如何提高过氧化氢的分解速率?请设计实验方案:_____。