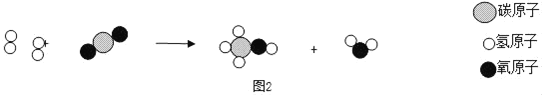
题目内容
【题目】某集团是一家以生产电缆类产品为主的国家大型企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.
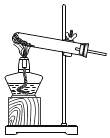
甲同学根据已学知识,提出了一套回收方案:
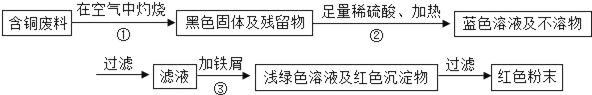
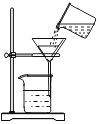
乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O22CuSO4+2H2O),于是他提出了另一套方案:
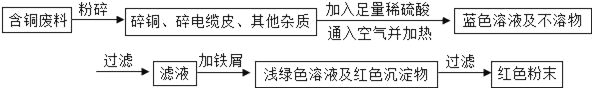
(1)甲方案的①②③三个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:①_____;②_____;③_____.
(2)从环保角度对两套方案的不同部分进行比较,你认为_____(填“甲”或“乙”)的方案更合理.理由是:_____.
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是:_____.
丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?”.请提出你的想法:_____.
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:_____、_____(“绿矾”溶解度随温度升高而增大).如果直接排放掉滤液,不仅造成了浪费,还会_____.
(5)若上述方案所用的稀硫酸溶质质量分数为36.8%,问每1000mL98%的浓硫酸(密度为1.84g/mL)能配制出这种稀硫酸_____g,需水_____mL(水的密度为1.0g/mL).在实验室中稀释浓硫酸时,是如何操作的:_____.
(6)根据乙同学查出的方程式(2Cu+2H2SO4+O2![]() 2CuSO4+2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜____克。(请写出计算过程,结果精确到0.1克)
2CuSO4+2H2O)计算:如果1000mL98%的浓硫酸(密度为1.84g/mL)稀释后全部参加了反应(假设硫酸不和碎电缆皮、其他杂质反应),所能处理的废料中含纯铜____克。(请写出计算过程,结果精确到0.1克)
【答案】2Cu+O2![]() 2CuO CuO+H2SO4═CuSO4+H2O Fe+CuSO4═FeSO4+Cu 乙 甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾 将Cu完全置换出来 过滤前在加适量的酸以除去剩余的铁粉 蒸发 降温 水污染 4900 3060 将浓硫酸沿玻璃棒加入水中 1177.6
2CuO CuO+H2SO4═CuSO4+H2O Fe+CuSO4═FeSO4+Cu 乙 甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾 将Cu完全置换出来 过滤前在加适量的酸以除去剩余的铁粉 蒸发 降温 水污染 4900 3060 将浓硫酸沿玻璃棒加入水中 1177.6
【解析】
“从含铜废料中回收铜”符合绿色化学的理念,再回收利用中,设计了两套方案,处理有关问题,并进行评价。甲方案中:发生的有关化学方程式为:①2Cu+O2![]() 2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu;但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;最后考查学生的计算能力及体验回收成果,增强成就感。
2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu;但“灼烧”会产生污染空气的气体、粉尘、烟雾,所以不如乙方案更合理;然后设计提取的有关问题;最后考查学生的计算能力及体验回收成果,增强成就感。
(1)有分析可知甲方案中:发生的有关化学方程式为:①2Cu+O2![]() 2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu;
2CuO;②CuO+H2SO4═CuSO4+H2O;③Fe+CuSO4═FeSO4+Cu;
(2)从环保的角度,乙方案更合理,甲方案的“灼烧”会产生污染空气的气体、粉尘、烟雾;
(3)加入略过量的铁屑的目的是“确保CuSO4用完”或“将Cu完全置换出来”;
(4)蒸发、降温都能使“绿矾”结晶出来,直接排放掉滤液,不仅造成了浪费,还会造成环境污染或水污染;
(5)设能配制出这种稀硫酸的质量为m,
1000mL×1.84g/mL×98%=36.8%m,m=4900g,则需要加入的水的质量为:4900g-1000mL×1.84g/mL=3060g,因水的密度是1g/mL,所以需要水的体积为3060mL。
硫酸稀释问题,操作为:将浓硫酸沿玻璃棒加入水中;
(6)设所能处理的废料中纯铜质量为x,
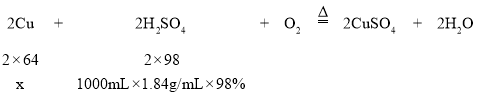
![]()
x=1177.6g,故填1177.6。

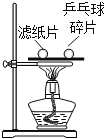
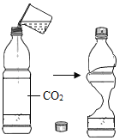
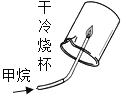
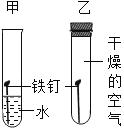
【题目】分析图示的四个实验,根据现象得出的结论,正确的是( )
|
|
|
|
A、可燃物燃烧需要温度达到着火点 | B、CO2与H2O反应生成H2CO3 | C、CH4燃烧生成CO2和H2O | D、铁钉生锈只需与H2O接触 |
A. AB. BC. CD. D