题目内容
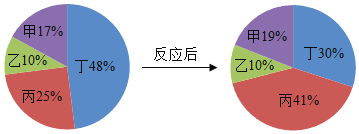
【题目】把一定质量的甲,乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量分数变化如图所示。下列说法中错误的是( )
A. 该反应为分解反应B. 乙可能是此反应的催化剂
C. 参加反应的甲、丁的质量之比为9:1D. 丁一定是化合物,甲、丙可能是单质
【答案】C
【解析】
由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数增加了19%-17%=2%,故甲是生成物;乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应;反应后丙的质量分数增加了41%-25%=16%,故是生成物;丁的质量分数减少了48%-30%=18%,丙是反应物。
A、该反应的生成物为甲和丙,反应物是丁,符合“一变多”的特征,属于分解反应,选项A正确,不符合题意;
B、乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,选项B正确,不符合题意;
C、参加反应的甲、丁的质量之比为2%∶18%=1∶9,选项C错误,符合题意;
D、该反应属于分解反应,丁是分解反应的反应物,一定是化合物,甲、丙是分解反应的生成物,可能是单质,选项D正确,不符合题意。故选C。

【题目】(1)实验室用过氧化氢与二氧化锰制取氧气的化学方程式为:______,加入二氧化锰是为了______。
(2)如表是某研究小组探究影响化学反应速率的因素的相关实验数据:(每次实验取用含碳酸钙60%的大理石10g.每次实验盐酸的用量为20mL,大理石中杂质不与盐酸反应)。
实验编号 | 温度/℃ | 大理石规格 | 盐酸的质量分数 | 完全反应的时间/s |
a | 20 | 粗颗粒 | 18.25% | 130 |
b | 粗颗粒 | 9.125% | 205 | |
c | 30 | 粗颗粒 | 18.25% | 63 |
d | 20 | 细颗粒 | 18.25% | 95 |
(实验目的)
①实验a和b探究大理石颗粒大小相同下盐酸的质量分数对该反应速率的影响,则实验b中的温度应该为______。
②实验a和c探究______对该反应速率的影响。
③实验a和______探究大理石颗粒大小对该反应速率的影响。
④根据表格中的数据写出2个与实验目的相对应的实验结论:______